 |
|
Viêm gan tự miễn
Có gì mới trong chẩn đoán và điều trị?
I.Giới thiệu
Viêm gan tự miễn là một bệnh gan dạng viêm hoại tử chưa giải quyết được, đặc trưng bởi một đáp ứng miễn dịch trực tiếp chống lại mô gan, dẫn đến sự hủy hoại nhu mô gan. Các chất chỉ điểm trong huyết thanh miễn dịch thường hiện diện, và bệnh thường tồn tại cùng với các rối loạn tự miễn khác kèm theo. Nguyên nhân của viêm gan tự miễn chưa được xác định rõ, nhưng bệnh có thể gây ra do một số hóa chất (ví dụ minocycline) và nhiễm virus (ví dụ viêm gan A). Với bản chất không đồng nhất của bệnh, viêm gan tự miễn đã được phân nhóm phụ thành 3 type dựa trên type kháng thể được phát hiện (Bảng 1). Sự thật là đối với hầu hết các bệnh tự miễn, phụ nữ chiếm đa số trong những bệnh nhân bị mắc viêm gan tự miễn, còn nam giới chỉ chiếm 10% đến 20% trong tất cả bệnh nhân. Tuy nhiên, các nghiên cứu mới đây trên những người bị viêm gan tự miễn type 1 không phát hiện sự khác biệt đáng kể về biểu hiện lâm sàng hoặc kết quả điều trị khi so sánh giữa phụ nữ và nam giới.
Bảng 1. Các đặc điểm lâm sàng của Viêm gan tự miễn, theo Type
Đặc điểm |
Type 1 |
Type 2 |
Type 3 |
Tự kháng thể |
ANA, SMA |
Kháng thể kháng LKM |
Kháng thể kháng SLA |
Tuổi khởi phát điển hình |
10+ |
2-14 |
30-50 |
Phụ nữ, % |
78 |
89 |
90 |
Bệnh miễn dịch đồng thời, % |
41 |
34 |
58 |
Kết hợp với HLA |
B8, DR3, DR4 |
B14, D23, C4AQO |
Không chắc chắn |
Tiến triển đến xơ gan, % |
45 |
82 |
75 |
ANA: Kháng thể kháng nhân; HLA: Kháng nguyên bạch cầu người, LKM: microsom gan/thận; SLA: Kháng nguyên gan hòa tan; SMA: Kháng thể kháng cơ trơn.
II.Các yếu tố di truyền
Các yếu tố di truyền dường như có liên quan trong sinh bệnh học của viêm gan tự miễn, và một giả thuyết hiện nay cho là viêm gan tự miễn gây ra do các yếu tố môi trường ở một vật chủ nhạy cảm do di truyền. Dường như không có một yếu tố di truyền đơn độc có khả năng gây viêm gan tự miễn; đúng hơn là nhiều gen tương tác tạo ra một vốn gen cho phép virus xâm nhiễm trong đó sự kết hợp một số gen làm tăng nguy cơ mắc bệnh và phenotype.
Ảnh hưởng di truyền mạnh nhất trên tính nhạy cảm đối với tự miễn dịch là phức hợp gen tương hợp mô chính. Các nghiên cứu trước đây đã nhận diện các gen đối với HLA-DRB1*0301 và HLA-DRB*0401 là những yếu tố xác định về tính nhạy cảm đối với viêm gan tự miễn type 1 ở bệnh nhân người Bắc Âu.Một nghiên cứu mới đây được tiến hành trên trẻ em bị viêm gan tự miễn type 2 đã phát hiện HLA-DQB1*0201 là yếu tố xác định tính nhạy cảm do di truyền sơ cấp đối với viêm gan tự miễn, trong khi vị trí của HLA-DR dường như liên quan nhiều hơn đến biểu hiện của tự kháng thể.
Cho đến nay, sự tìm kiếm các gen ngoài phức hợp gen tương hợp mô chính chưa phát hiện bất kỳ sự liên quan nào rõ rệt. Yếu tố hoại tử khối u α (TNF-α) và các alen yếu tố bổ thể C4 có liên quan với viêm gan tự miễn ở bệnh nhân da trắng, nhưng cả hai gen đều cho thấy mất cân bằng liên kết rõ rệt với haplotype HLA A1-B8-DR3. Gen có ảnh hưởng nhiều nhất trong sinh bệnh học của viêm gan tự miễn type 1 ở bệnh nhân người Nhật là HLA-DRB1. Các gen khác trong vùng gen kháng nguyên bạch cầu người (HLA), bao gồm TNF-α, cho thấy ít liên quan hoặc không liên quan với tính nhạy cảm đối với viêm gan tự miễn type 1. Viêm gan tự miễn không cổ điển có thể xảy ra như một phần của hội chứng bệnh lý đa tuyến nội tiết-bệnh nấm candida-loạn dưỡng ngoại bì tự miễn, gây ra do đột biến gen điều hòa tự miễn (AIRE). Tuy nhiên, đột biến và/hoặc tính đa hình về AIRE chưa được phát hiện ở bệnh nhân bị bệnh gan tự miễn cổ điển.
III.Tiêu chuẩn chẩn đoán viêm gan tự miễn
Biểu hiện lâm sàng của viêm gan tự miễn ở mức từ không có triệu chứng (gặp đến 25% trường hợp, bệnh được phát hiện tình cờ khi các enzyme gan bất thường được tìm thấy qua khám sàng lọc) đến một tiến trình bệnh nặng, đôi khi tối cấp. Cũng như với các dạng bệnh gan mạn tính khác, hầu hết bệnh nhân viêm gan tự miễn có các triệu chứng điển hình gồm mệt mỏi, vàng da dao động, đau bụng ở 1/4 trên bên phải, và đau khớp. Ngoài ra, đã quan sát thấy tăng tần suất bệnh tự miễn ngoài gan ở những bệnh nhân viêm gan tự miễn.
Do các dấu hiệu và triệu chứng của viêm gan tự miễn không đặc hiệu và do không có sẵn xét nghiệm đặc hiệu đối với viêm gan tự miễn, một nhóm các chuyên gia quốc tế về viêm gan gọi là nhóm viêm gan tự miễn quốc tế đã thiết lập một bộ tiêu chuẩn chẩn đoán viêm gan tự miễn dựa trên sự đồng thuận.Trong hầu hết trường hợp, những tiêu chuẩn này đủ để chẩn đoán viêm gan tự miễn dựa trên sinh hóa huyết thanh, nồng độ glubulin miễn dịch trong huyết thanh, nồng độ tự kháng thể trong huyết thanh, các chất chỉ điểm virus, mô học về gan, và các yếu tố bệnh nguyên khác (Bảng 2).
1.Đánh giá về sinh hóa
Trong đa số trường hợp viêm gan tự miễn, đánh giá về sinh hóa đã phát hiện một mô hình được đặc trưng bởi sự tăng rõ rệt nồng độ aminotransferase so với nồng độ bilirubin và phosphatase kiềm và tăng rõ rệt về các gamma-globulin, đặc biệt là nồng độ IgG trong huyết thanh.
2.Tự kháng thể
Tự kháng thể là một trong những đặc điểm phân biệt của viêm gan tự miễn. Kháng thể kháng nhân, kháng thể kháng cơ trơn (SMA), và kháng thể kháng microsom 1 của gan/thận (LKM1) là các thành phần chủ chốt để chẩn đoán và phân loại viêm gan tự miễn và cần được thử ở những bệnh nhân nghi ngờ có tình trạng này (Bảng 3).
Bảng 2. Tiêu chuẩn chẩn đoán quốc tế để Chẩn đoán Viêm gan tự miễn*
|
Điểm |
Giới |
|
■ Nam |
+2 |
■ Nữ |
0 |
Sinh hóa huyết thanh, tỷ số tăng phosphatase kiềm huyết thanh so với amino transferase |
|
■ > 3,0 |
-2 |
■ > 1,5 – 3,0 |
0 |
■ < 1,5 |
+2 |
Globulin huyết thanh (globulin huyết thanh toàn phần, gamma-globulin, hoặc IgG), x ULN |
|
■ > 2,0 |
+3 |
■ 1,5 – 2,0 |
+2 |
■ 1,0 – 1,5 |
+1 |
■ < 1,0 |
0 |
Tự kháng thể kháng nhân, kháng cơ trơn, hoặc kháng LKM1, hiệu giᆠ|
|
■ > 1: 80 |
+3 |
■ 1: 80 |
+2 |
■ 1: 40 |
+1 |
■ < 1:40 |
0 |
Kháng thể kháng ty lạp thể |
|
■ Dương tính |
-4 |
■ Âm tính |
0 |
Huyết thanh dương tính đối với các kháng thể khác (pANCA, kháng thể kháng LC1, kháng SLA/LP, kháng ASGPR, kháng sulfatide) |
+2 |
Chất chỉ điểm viêm gan virus (viêm gan A, B, hoặc C) |
|
■ Âm tính |
+3 |
■ Dương tính |
-3 |
Tiền sử dùng thuốc |
|
■ Có |
-4 |
■ Không |
+1 |
Lượng rượu uống trung bình, g/ngày |
|
■ < 25 |
+2 |
■ > 60 |
-2 |
Có yếu tố di truyền (HLA, DR3, hoặc DR4) |
+1 |
Có các rối loạn tự miễn khác |
+2 |
Mô học về gan |
|
■ Viêm gan bề mặt |
+3 |
■ Thâm nhiễm tế bào lympho chiếm ưu thế |
+1 |
■ Hình hoa hồng tế bào gan |
+1 |
■ Không có trường hợp nào ở trên |
-5 |
■ Thay đổi về mật |
-3 |
■ Các thay đổi khác |
-3 |
Đáp ứng với điều trị |
|
■ Hoàn toàn |
+2 |
■ Tái phát |
+3 |
ASGPR: thụ thể asialoglycoprotein; IgG: globulin miễn dịch G; LC1: cytosol type 1 của gan; LKM1: microsome type 1 của gan, thận; pANCA: kháng thể bào tương kháng bạch cầu trung tính quanh nhân; SLA/LP: kháng nguyên gan hòa tan/kháng nguyên tụy-gan; ULN: giới hạn trên của mức bình thường.
* Trước khi điều trị, chẩn đoán xác định cần điểm > 15; sau khi điều trị, chẩn đoán xác định cần điểm > 17.
† Bằng phương pháp miễn dịch huỳnh quang trên mô của loài gặm nhấm.
Bảng 3. Các tự kháng thể liên quan với Viêm gan tự miễn
|
Chú thích |
|
ANA |
■ Không đặc hiệu |
|
SMA |
■ Không đặc hiệu |
|
Kháng thể kháng LKM1 |
■ Các đích CYP2D6 |
|
Kháng thể kháng LKM2 |
■ Gây ra do ticrynafen (hiện nay không còn trên thị trường) |
|
Kháng thể kháng LKM3 |
■ Các đích UGT1A |
|
LC1 |
■ Các đích enzyme đặc hiệu của gan: formiminotranferase cyclodeaminase |
|
pANCA |
■ Không đặc hiệu |
|
SLA/LP |
■ Các đích protein kết hợp tRNA ức chế-UGA (UGA-suppessor |
|
AFLD: bệnh gan nhiễm mỡ do rượu; ANA: kháng thể kháng nhân; CYP2D6: cytochrome P450 2D6; LKM: kháng thể kháng microsom gan, thận; NAFLD: bệnh gan nhiễm mỡ không do rượu; pANCA: kháng thể bào tương kháng bạch cầu trung tính quanh nhân; PBC: xơ gan mật nguyên phát; PSC: viêm đường mật xơ cứng nguyên phát; SLA/LP: kháng nguyên gan hòa tan/kháng nguyên tụy-gan; SMA: kháng thể kháng cơ trơn; tRNA: RNA vận chuyển; UGT1A: uridine 5’-diphosphate glucuronosyltransferase.
Kháng thể kháng nhân là những tự kháng thể đầu tiên liên quan với viêm gan tự miễn. Tuy nhiên, kháng thể kháng nhân (ANA) cũng ngẫu nhiên trở thành chất chỉ điểm không đặc hiệu nhiều nhất đối với bệnh này, vì chúng có thể được tìm thấy trong xơ gan mật nguyên phát (PBC), viêm xơ chai đường mật nguyên phát (PSC), viêm gan virus, viêm, viêm gan do thuốc, và bệnh gan nhiễm mỡ do rượu và không do rượu.
3.Tính không đặc hiệu của kháng thể kháng nhân dương tính.
Cần phải lưu ý về một số xem xét liên quan đến vai trò của tự kháng thể trong sinh bệnh học và chẩn đoán viêm gan tự miễn. Nói chung, tự kháng thể không đặc hiệu đối với viêm gan tự miễn. Các tự kháng thể đặc hiệu ít nhất trong việc chẩn đoán viêm gan tự miễn là các kháng thể chống lại kháng nguyên nhân (tức là ANA). Kháng thể chống lại kháng nguyên nhân là một dấu hiệu về rối loạn tự miễn hệ thống, như bệnh thấp khớp, lupus ban đỏ hệ thống, viêm khớp dạng thấp, và viêm da cơ. Các mức biểu hiện của tự kháng thể có thể thay đổi đáng kể trong suốt tiến trình của bệnh. Một hiệu giá kháng thể thấp không loại trừ chẩn đoán viêm gan tự miễn, hiệu giá kháng thể cao cũng không dùng để thiết lập chẩn đoán nếu không có các dấu chứng hỗ trợ khác; các hiệu giá tự kháng thể bổ sung các đặc điểm khác để hỗ trợ cho chẩn đoán. Các tự kháng thể tìm thấy trong viêm gan tự miễn dường như không gây ra bệnh; và ở người lớn dường như chúng không làm thay đổi đáp ứng đối với điều trị. Tuy nhiên, ở trẻ em, các hiệu giá tự kháng thể và nồng độ IgG phản ánh sát hoạt tính bệnh và vì vậy hữu ích như là những chất chỉ điểm trong thời gian giám sát điều trị.
Có nhiều chứng cứ thực nghiệm cho thấy các tự kháng thể là do đáp ứng miễn dịch bình thường được điều khiển bởi tự các thành phần. Các tự kháng thể mang những dấu hiệu của một đáp ứng miễn dịch thông thường đối với một kháng nguyên ngoại lai là một nhóm chuyển từ globulin miễn dịch M sang globulin miễn dịch G (IgG), các nhóm kháng thể và phân nhóm khác, đột biến các gen kháng thể theo thời gian, tính đặc hiệu cấp độ cao, và sự thuần thục ái lực. Những yếu tố có thể ảnh hưởng đến sự lựa chọn các tự kháng nguyên bao gồm các đặc điểm về cấu trúc của protein kháng nguyên (tức là bề mặt tải trọng cao, các yếu tố bề mặt lặp lại, sự có mặt của dây xoắn, hoặc acid nucleic dạng kết hợp), sự dị hóa và chết kháng nguyên sau khi chết tế bào (tức là phân cắt bởi enzyme, sự biến đổi sau dịch mã, sự khu trú ở bọt tế bào chất trong sự chết tế bào theo chương trình, sự giải phóng vào khoang ngoại bào), và nồng độ và/hoặc vi môi trường của protein kháng nguyên (tức là nồng độ tại chỗ cao do tăng điều hòa biểu hiện gen, sự kéo dài, hoặc các yếu tố đặc hiệu mô tại chỗ). Thông thường các đặc điểm về cấu trúc cần thiết là đặc trưng của kháng nguyên nhân, có thể giải thích cho tần suất cao của ANA trong các bệnh tự miễn bao gồm cả viêm gan tự miễn.
Kháng thể kháng cơ trơn là một tự kháng thể không đặc hiệu trực tiếp chống lại các protein bộ xương tế bào, như actin, troponin, và tropomyosin, và thường xảy ra ở hiệu giá cao liên quan với ANA. Kháng thể kháng cơ trơn cũng được tìm thấy trong bệnh gan tiến triển có bệnh nguyên khác và các rối loạn thấp khớp.
Kháng thể kháng LKM1 được phát hiện đầu tiên vào năm 1973 bằng phương pháp miễn dịch huỳnh quang gián tiếp và tái hoạt với ống thận xa và bào tương của tế bào gan. Đích phân tử của kháng thể kháng LKM1 là cytochrome P450 2D6 (CYP2D6). Các kháng thể kháng LKM1 nhận diện các chuỗi acid amin ngắn trên CYP2D6 theo cách có thứ bậc. Điều thú vị là một nghiên cứu mới đây điều tra tính miễn dịch tế bào chống lại CYP2D6 đã quan sát thấy một sự chồng lên nhau giữa các chuỗi gây đáp ứng tế bào B và tế bào T, cũng như mối liên quan giữa đáp ứng tế bào T với các chất chỉ điểm sinh hóa và mô học về hoạt tính viêm gan tự miễn.
Mặc dù các kháng thể kháng LKM1 được xem là một chất chỉ điểm trong huyết thanh về viêm gan tự miễn tương đối đặc hiệu, 5% đến 10% bệnh nhân bị viêm gan C mạn tính cũng dương tính với kháng thể kháng LKM1. Mới đây, một phương pháp mới kết hợp sự chiếm chỗ thực khuẩn thể và việc nhận diện các cặp có ý nghĩa thống kê đã được sử dụng để nhận diện các epitope CYP2D6 dạng cấu hình. Epitope dạng cấu hình được nhắm đến bởi các kháng thể hiện diện ở bệnh nhân bị nhiễm virus viêm gan C khu trú trong cùng 1 vùng như epitope dạng thẳng chính được nhận diện bởi bệnh nhân viêm gan tự miễn. Điều quan trọng là những kháng thể này phản ứng chéo với protein của virus viêm gan C, cho thấy là chúng có thể là kết quả của sự bắt chước phân tử ở mức tế bào B.
Các kháng thể kháng LKM2 trực tiếp chống lại CYP2C9 và được tạo ra trong viêm gan do ticrynafen là một thuốc chống tăng huyết áp đã được rút khỏi thị trường từ lâu. Các kháng thể kháng LKM3 được phát hiện ở khoảng 10% bệnh nhân bị viêm gan tự miễn type 2, đơn độc hoặc phối hợp với kháng thể kháng LKM1. Chúng trực tiếp chống lại UGT1A thuộc họ enzyme chuyển hóa thuốc khu trú ở lưới nội chất.
Những bệnh nhân không có những tự kháng thể nói trên có thể được thử nghiệm để tìm các tự kháng thể đã được xác định rõ khác. Các kháng thể chống lại LC1, pANCA, và SLA/LP có thể hữu ích cho việc mở rộng chẩn đoán viêm gan tự miễn để chọn lọc bệnh nhân. Các kháng thể kháng SLA/LP có thể được phát hiện ở khoảng 10% đến 30% trong tất cả bệnh nhân bị viêm gan tự miễn. Từ quan điểm lâm sàng, một số nghiên cứu đã xác nhận quan sát ban đầu là bệnh nhân có kháng thể kháng SLA/LP cho thấy một tiến trình viêm gan tự miễn nặng hơn. Tuy nhiên, ở những bệnh nhân người Nhật bị viêm gan tự miễn type 1, các kháng thể kháng SLA/LP chỉ được phát hiện ở tần suất thấp và không ảnh hưởng đáng kể đến các đặc điểm lâm sàng của bệnh.
IV.Chẩn đoán phân biệt
Một khi nghi ngờ viêm gan tự miễn, cần phải tiến hành đánh giá về chẩn đoán thêm để loại trừ viêm gan virus mạn tính, các bệnh di truyền và các bệnh tự miễn khác - đặc biệt là xơ gan mật nguyên phát (PBC) và viêm đường mật xơ chai nguyên phát (PSC).
1.Đặc điểm của Xơ gan mật nguyên phát (PBC)
Xơ gan mật nguyên phát là một bệnh gan ứ mật mạn tính ảnh hưởng chủ yếu trên phụ nữ, ngược với nam giới (tỷ số 9:1). Đây có lẽ là một bệnh tự miễn và được đặc trưng bởi sự hủy hoại lâu dài các ống mật nhỏ trong gan. Triệu chứng lâm sàng của xơ gan mật nguyên phát điển hình bao gồm mệt mỏi, ngứa và vàng da. Trong một số trường hợp, có xuất hiện ban vàng. Các nồng độ phosphatase kiềm và bilirubin thường cao hơn nhiều trong xơ gan mật nguyên phát so với viêm gan tự miễn. Các tự kháng thể có thể phát hiện được một cách điển hình và hơn 90% bệnh nhân phát triển các kháng thể chống lại phức hợp pyruvate dehydrogenase khu trú ở ty lạp thể. Vì vậy, những kháng thể này được gọi là kháng thể kháng ty lạp thể (AMA). Những trường hợp âm tính với kháng thể được gọi là AMA của xơ gan mật nguyên phát có lẽ thứ phát do các hạn chế về phương pháp phát hiện. Các thử nghiệm tạo hạt nhạy hơn đã được phát triển và có thể phát hiện AMA ở các mẫu huyết thanh âm tính với AMA khác. Kháng thể kháng nhân và kháng thể kháng Sp100 cũng có thể được phát hiện trong xơ gan mật nguyên phát. Mô học cũng quan trọng trong chẩn đoán và phân giai đoạn xơ gan mật nguyên phát. Giai đoạn 1, hoặc giai đoạn ở khoảng cửa, được đặc trưng bởi viêm khoảng cửa và tổn thương ống mật khó thấy, và u hạt thường có thể phát hiện được. Giai đoạn 2, hoặc giai đoạn quanh khoảng cửa, tam chứng tăng lên với xơ hóa quanh khoảng cửa và/hoặc viêm. Một dấu hiệu điển hình là tăng sinh các ống mật nhỏ. Giai đoạn 3 là giai đoạn vách, được đặc trưng bởi vách xơ. Giai đoạn 4 được gọi là xơ gan mật, xuất hiện các u nhỏ kiểu vòng hoa hoặc kiểu lắp hình. Xơ gan mật nguyên phát được điều trị bằng acid ursodeoxycholic, thường làm giảm ứ mật và cải thiện các xét nghiệm chức năng gan. Những bệnh nhân không đáp ứng với điều trị bằng thuốc có thể được ghép gan khi bị bệnh gan tiến triển.
2.Đặc điểm của Viêm xơ chai đường mật nguyên phát (PSC)
Viêm đường mật xơ chai nguyên phát bao gồm sự hủy hoại liên tục các ống mật trong gan và ngoài gan. Bệnh ảnh hưởng đến nam giới nhiều hơn (64%) so với xơ gan mật nguyên phát và viêm gan tự miễn. Các triệu chứng lâm sàng thường tương tự như các bệnh gan khác, bao gồm mệt mỏi, vàng da và ngứa. Kém hấp thu và phân mỡ có thể rõ rệt. Cũng như trong xơ gan mật nguyên phát (PBC), các xét nghiệm chức năng gan thường phát hiện nồng độ phosphatase kiềm và bilirubin tăng. Khoảng 74% đến 92% bệnh nhân bị viêm đường mật xơ cứng nguyên phát có bệnh viêm ruột đồng thời, đặc biệt là viêm loét đại tràng. Bệnh nhân viêm đường mật xơ cứng nguyên phát không phát triển các tự kháng thể đặc hiệu của bệnh, và pANCA có thể được phát hiện đến 75% trường hợp. Thông thường, chẩn đoán viêm đường mật xơ cứng nguyên phát được thiết lập bằng cách chụp đường mật bằng cộng hưởng từ hoặc chụp đường mật ngược dòng qua nội soi (ERC), phát hiện những thay đổi đặc trưng ở ống mật. Các đặc điểm mô học đặc trưng của viêm đường mật xơ cứng nguyên phát là xơ hóa quanh ống mật đồng tâm, còn được gọi là hình vỏ củ hành (onion-skinning), có thể tiến triển đến hẹp và tắc ống dẫn mật. Ức chế miễn dịch không phải là phương thức điều trị chuẩn và thậm chí có thể làm thay đổi hoạt tính và tiến triển của bệnh. Cho đến nay trị liệu hiệu quả nhất là dùng liều cao acid ursodeoxycholic và chụp đường mật ngược dòng qua nội soi (ERC) lặp lại, có thể bao gồm việc đặt stent các ống mật lớn và có thể cần mở các chỗ hẹp nhất. Chụp đường mật ngược dòng qua nội soi cũng quan trọng trong việc theo dõi diễn tiến bệnh để phát hiện loạn sản ống mật. Trong những trường hợp này, ghép gan là sự lựa chọn duy nhất để tránh phát triển ung thư đường mật.
Sinh thiết gan qua da cần được thực hiện khi loại trừ những nguyên nhân này và nguyên nhân khác của bệnh gan khỏi chẩn đoán viêm gan tự miễn vì đánh giá về mô học là quan trọng để phân loại và phân giai đoạn cũng như để theo dõi điều trị. Các đặc điểm về mô học thường bao gồm viêm gan bề mặt, thâm nhiễm tế bào lympho, tích tụ tương bào, và hoại tử từng phần. Ở một số bệnh nhân bị viêm gan tự miễn, đã gặp xơ hóa khi sinh thiết lần đầu tiên. Với bệnh tiến triển có thể xảy ra xơ hóa bắt cầu, xơ hóa tất cả thùy, và xơ hóa nhiều thùy có thể xảy ra, cuối cùng dẫn đến xơ gan. Đôi khi viêm gan tự miễn biểu hiện với hình ảnh ứ mật nhiều hơn, tuy nhiên hầu hết bệnh nhân có các đặc điểm về mô học và sinh hóa về tổn thương ống mật đáp ứng các tiêu chuẩn quốc tế đối với viêm gan tự miễn của bệnh gan ứ mật và đáp ứng tốt với điều trị corticosteroid.
V.Điều trị thông thường và Các phương thức Điều trị duy trì đối với bệnh nhân bị viêm gan tự miễn
Viêm gan tự miễn là bệnh gan mạn tính đầu tiên mà liệu pháp dùng thuốc đã cải thiện sự sống còn. Mục tiêu chính của điều trị viêm gan tự miễn là làm thuyên giảm các triệu chứng trên lâm sàng, làm tiêu viêm và hết tổn thương tế bào gan về mặt sinh hóa và mô học. Mục tiêu cuối cùng là duy trì sự thuyên giảm bệnh mà không cần điều trị bằng thuốc. Sự thuyên giảm có thể được xác định khi không còn các triệu chứng lâm sàng; bình thường hóa các nồng độ aminotransferase huyết thanh, bilirubin huyết thanh, gamma-globulin/IgG huyết thanh; và cải thiện về mô học của gan về mức bình thường hoặc chỉ còn viêm gan khoảng cửa nhẹ. Điều này đã đạt được ở khoảng 80% bệnh nhân được điều trị (Hình). Cần bắt đầu điều trị ở tất cả bệnh nhân có khởi phát bệnh nặng, được đặc trưng bởi nồng độ aminotransferase vượt quá 5-10 lần giới hạn trên của mức bình thường và/hoặc có dấu hiệu mô học về sự bắt cầu hoặc hoại tử nhiều thùy. Những bệnh nhân không có triệu chứng có thể không cần liệu pháp ức chế miễn dịch và có tiên lượng tốt. Tuy nhiên, những bệnh nhân không dùng liệu pháp ức chế miễn dịch cần được theo dõi sát về dấu hiệu tiến triển bệnh. Nói chung, quyết định điều trị cho bệnh nhân bị viêm gan tự miễn phải được cân nhắc với các nguy cơ khi dùng thuốc.
Các hướng dẫn của Hiệp hội Nghiên cứu bệnh gan Mỹ (AASLD) khuyến cáo dùng prednisone phối hợp với azathioprine như một điều trị khởi đầu được ưa thích hơn đối với viêm gan tự miễn. Tuy nhiên, một liều prednisone đầy đủ (0,5 – 1,0 mg/kg thể trọng) đơn độc có thể đủ để dẫn đến sự cải thiện về lâm sàng, xét nghiệm và mô học và do đó làm thuyên giảm bệnh. Viêm gan tự miễn đáp ứng một cách đặc trưng với liệu pháp này, và tiên lượng tốt chừng nào mà việc quản lý thích hợp vẫn còn được thực hiện.
AASLD khuyến cáo tất cả bệnh nhân viêm gan tự miễn điều trị bằng prednisone đơn độc hoặc phối hợp với azathioprine cần được theo dõi về sự phát triển các tác dụng phụ liên quan đến việc sử dụng thuốc; việc điều trị đã bị ngừng lại ở khoảng 10% bệnh nhân do các tác dụng phụ. Cách tiếp cận hợp lý trong trường hợp này là điều trị corticosteroid hoặc azathioprine đơn độc bất cứ lúc nào dung nạp được với một liều kiểm soát được hoạt tính của bệnh. Có thể xem xét dùng azathioprine đơn độc ở bệnh nhân có nguy cơ cao về các tác dụng phụ của corticosteroid. Tuy nhiên, điều trị phối hợp nói chung được ưa thích hơn do các dữ liệu thuyết phục ghi nhận hiệu quả của corticosteroid như là một điều trị khởi đầu.
Cách tiếp cận điều trị viêm gan tự miễn và sự cần thiết dùng thuốc thay thế.
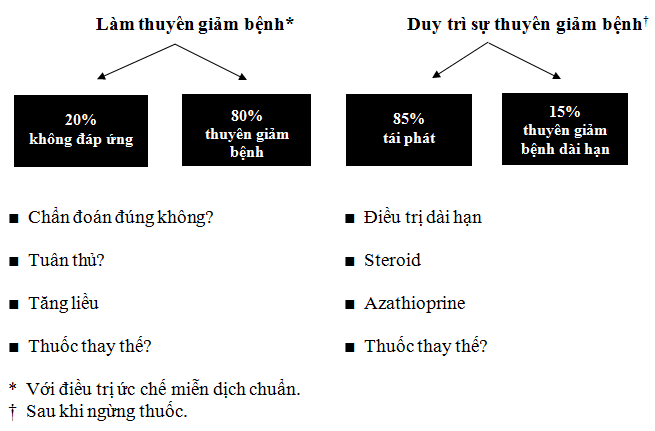
Cần tiếp tục điều trị cho đến khi thuyên giảm bệnh; được xác định là diễn tiến đến dạng không triệu chứng về lâm sàng, với các xét nghiệm bình thường ngoại trừ đối với dạng có xét nghiệm enzyme gan bình thường và mô học bình thường. Có thể ngừng điều trị bất cứ lúc nào do các tác dụng phụ liên quan với việc không dung nạp điều trị hoặc thất bại điều trị rõ ràng. Nói chung, khuyến cáo ngừng corticosteroid từ từ qua một thời gian dài với liều prednisone giảm 5-10 mg mỗi tuần đến 30 mg/ngày, sau đó tiếp theo bằng sự giảm từng 2,5 mg mỗi tuần cho đến khi ngừng thuốc hoàn toàn.
Liều prednisone duy trì điển hình là 5-10 mg/ngày, ở những bệnh nhân đang dùng liệu pháp phối hợp, điều trị duy trì bằng azathioprine đơn độc đáng mong muốn. Liều azathioprine có thể tăng đến 2 mg/kg/ngày và liều prednisone giảm từng 2,5 mg mỗi tháng cho đến khi ngừng thuốc hoàn toàn. Ở những bệnh nhân đang dùng prednisone đơn độc, trong số những người mà điều trị duy trì bằng azathioprine đơn độc đáng mong muốn, có thể cộng thêm azathioprine 2 mg/kg/ngày, sau liều này có thể giảm liều prednisone từng 2,5 mg mỗi tháng. Mặc dù chưa có sự đồng thuận về việc nên tiếp tục điều trị duy trì như vậy trong bao lâu, nhưng người ta khuyến cáo điều trị duy trì nên được tiếp tục ít nhất 6 tháng sau khi có được sự cải thiện về mô học.
Sự tranh luận về thời gian điều trị tối ưu vẫn còn tiếp tục, nhưng một nghiên cứu đã cho thấy là xác suất thuyên giảm kéo dài không cần điều trị cao hơn ở những bệnh nhân đã dùng liệp pháp ức chế miễn dịch liên tục trong 4 năm so với 2 năm hoặc dưới 2 năm (67% so với 17% và so với 10% tương ứng).Krawitt khuyến cáo điều trị duy trì dài hạn đối với hầu hết bệnh nhân bị viêm gan tự miễn và ngay cả điều trị duy trì suốt đời đối với người lớn và trẻ em bị xơ gan vào lúc sinh thiết đầu tiên, đặc biệt ở trẻ em bị viêm gan tự miễn type 2.
Sự tiêu viêm gan có thể xảy ra trong thời gian dùng liệu pháp ức chế miễn dịch, làm giảm nguy cơ tái phát khoảng 20% sau khi ngừng điều trị, Nếu sinh thiết gan vẫn cho thấy còn viêm gan khoảng cửa, tái phát sẽ xảy ra ở 50% bệnh nhân trong vòng 6 tháng sau khi ngừng thuốc. Ở những bệnh nhân tiến triển đến xơ gan hoặc những người cho thấy các dấu hiệu viêm gan bề mặt, tái phát lúc nào cũng được quan sát thấy vào giai đoạn cuối của điều trị ức chế miễn dịch. Nhìn chung, đáp ứng kéo dài đạt được chỉ vào khoảng 20% trong tất cả bệnh nhân vào giai đoạn cuối của điều trị ức chế miễn dịch. Tuy nhiên, đã có một số thuốc khác, đặc biệt là từ trường hợp ghép gan, có thể cho sự ức chế miễn dịch cao hơn và được dung nạp tốt hơn prednisone và azathioprine.
VI.Các thuốc thay thế ở bệnh nhân viêm gan tự miễn đáp ứng kém với Prednisone và Azathioprine
Nhiều thuốc khác nhau đã được thử nghiệm về khả năng điều chỉnh viêm gan tự miễn trong các thử nghiệm lâm sàng với các mức độ hiệu quả khác nhau (Bảng 4).
Bảng 4. Trị liệu chuẩn và trị liệu mới đối với Viêm gan tự miễn
|
■ Prednisone ± azathioprine |
Trị liệu ức chế miễn dịch thay thế |
■ Chất ức chế calcineurin |
• Cyclosporin A |
• Tacrolimus |
■ Chất ức chế mTOR |
• Sirolimus (aka rapamycin) |
■ Corticosteroid thế hệ thứ 2 |
• Budenoside |
• Deflazacort |
■ Thuốc khác |
• Mycophenolate mofetil |
• Cyclophospham |
• Methotrexate |
|
■ Acid ursodeoxycholie |
mTOR: đích của rapamycin ở động vật có vú.
1.Chất ức chế calcineurin
Chất ức chế calcineurin (ví dụ cyclosporine, tacrolimus) tác động trên cyclophyllin (hoặc immunophillin) là những protein cytosol của tế bào lympho. Sự ức chế calcineurin chặn sự phiên mã interleukin-2 là yếu tố chính liên quan đến sự tăng sinh tế bào T hoạt hóa. Cyclosporine là một peptide nhỏ từ nấm gồm 11 acid amin và là một trong những thuốc ức chế miễn dịch được sử dụng rộng rãi nhất. Tacrolimus là một macrolide lactone từ nấm. Nó mạnh hơn cyclosporine và dường như có tác dụng phụ ít rõ rệt hơn. Sirolimus, còn được biết là rapamycin là một macrolide lactone tác động hơi khác so với cycloporin và tacrolimus. Mặc dù sirolimus gắn kết với cùng thụ thể như tacrolimus, phức hợp này không ức chế calcineurin và do đó có thể tác động hiệp đồng với các chất ức chế calcineurin.
2.Thuốc kìm tế bào
Thuốc kìm tế bào, bao gồm các thuốc alkyl hóa và thuốc kháng chuyển hóa, được sử dụng để ức chế sự phân chia tế bào. Các liều thuốc kìm tế bào nhỏ hơn thường được dùng trong trị liệu miễn dịch so với các liều được dùng trong điều trị bệnh ác tính. Cyclophosphamide là một thuốc alkyl hóa và được sử dụng trong điều trị một số bệnh tự miễn. Các thuốc kháng chuyển hóa (ví dụ methotrexate, azathioprine, mercaptopurine) can thiệp vào sự tổng hợp các acid nucleic. Methotrexate là một chất tương tự acid folic, ngăn cản sự tổng hợp tetrahydrofolate bằng cách gắn kết với dihydrofolate reductase. Mercaptopurine tác động như một chất tương tự purine, dẫn đến ức chế sự tổng hợp DNA. Azathioprine bị phân cắt không do enzyme để tạo thành chất chuyển hóa có hoạt tính là mercaptopurine.
Mycophenolate mofetil được chuyển hóa ở gan thành acid mycophenolic nửa hoạt tính. Nó là một chất ức chế inosine monophosphate dehydrogenase, là một enzyme kiểm soát tốc độ tổng hợp guanine monophosphate theo đường tổng hợp purine mới. Nó ảnh hưởng đến sự tăng sinh của tế bào lympho B và T.
3.Kháng thể đơn dòng
Trong những năm gần đây, các kháng thể đơn dòng hướng trực tiếp đến các kháng nguyên đặc hiệu đã được phát triển. Khả năng của chúng trong điều trị ghép gan, và điều trị các rối loạn tự miễn hiện nay đang được nghiên cứu, có tên là kháng CD3.
VII.Ghép gan trong trường hợp Viêm gan tự miễn
Ghép gan là lựa chọn cứu mạng duy nhất đối với khoảng 10% bệnh nhân bị viêm gan tự miễn không đáp ứng với bất kỳ điều trị nào. Chỉ định ghép gan trong viêm gan tự miễn giống với chỉ định ở những bệnh nhân bị bệnh gan mạn tính giai đoạn cuối khác. Các đối tượng cho việc ghép gan là những bệnh nhân thường không cho thấy đáp ứng sớm hơn sau 6 tháng điều trị ức chế miễn dịch và những người không đạt được sự thuyên giảm trong vòng 3 năm trị liệu liên tục.Kết quả dài hạn sau khi ghép gan đối với viêm gan tự miễn rất tốt và tốt trong phạm vi các chỉ định khác cho việc ghép gan.
Các nghiên cứu đã được công bố trong những năm qua cho thấy là tỷ lệ tái phát viêm gan tự miễn sau ghép gan ở mức từ 10% đến 35%; nguy cơ tái phát viêm gan tự miễn có thể cao bằng 68% sau 5 năm theo dõi. Yếu tố nguy cơ đáng kể đối với tái phát viêm gan tự miễn sau ghép gan chưa được nhận biết. Prednisone, dùng đơn độc hoặc phối hợp với azathioprine vẫn là trị liệu lựa chọn đối với viêm gan tự miễn tái phát trong trường hợp này. Ở những bệnh nhân bị viêm gan sau ghép gan không đáp ứng với điều trị bằng prednisone liều tăng và thêm azathioprine hoặc mycophenolate mofetil, việc bổ sung sirolimus sau đó (còn được biết là rapamycin) đã cho thấy tạo ra đáp ứng thành công. Một số nghiên cứu theo dõi cho thấy là bệnh nhân bị viêm gan tự miễn tái phát có nguy cơ phát triển xơ gan sau ghép cùng loài khác gen, cần phải ghép lại. Một số bệnh nhân lại còn phát triển tái phát viêm gan tự miễn trong khi ghép lần thứ 2.
Đã có báo cáo về một tình trạng bệnh với các đặc điểm của viêm gan tự miễn đáp ứng với steroid ở những bệnh nhân đã được ghép gan đối với các chỉ định khác so với bệnh gan tự miễn. Trong một nghiên cứu ban đầu công bố vào năm 1998, viêm gan tự miễn mới (de novo) sau ghép gan được mô tả đầu tiên ở trẻ em. Đã có báo cáo bởi một số nhóm khác về một bệnh cảnh tương tự sau ghép gan cả ở trẻ em và người lớn. Tuy nhiên, trẻ em dường như có nguy cơ cao hơn đối với viêm gan tự miễn/viêm gan miễn dịch mới. Sinh bệnh học của tình trạng này chưa được xác định, và đến nay chưa có các tiêu chuẩn chẩn đoán được thiết lập đối với viêm gan tự miễn/viêm gan miễn dịch mới. Vì vậy, chẩn đoán viêm gan tự miễn/viêm gan miễn dịch mới chỉ có thể dựa trên cùng tiêu chuẩn như đối với viêm gan tự miễn và viêm gan tự miễn tái phát. Việc tăng nhận thức là điều trị bằng prednisone và azathioprine thành công trong viêm gan tự miễn/viêm gan miễn dịch mới đã dẫn đến sự chấp nhận mảnh ghép rất tốt và cải thiện sự sống còn cho bệnh nhân.
VIII.Kết luận và tóm tắt
Điều trị hiện hành và điều trị mới đối với viêm gan tự miễn đã làm thay đổi lớn viễn cảnh đối với những bệnh nhân bị bệnh này. Các kỹ thuật điều biến miễn dịch hiện nay đã làm cho nó trở thành một bệnh có thể điều trị được và làm giảm số bệnh nhân nói chung cần ghép gan cuối cùng. Chẩn đoán phân biệt cẩn thận có thể xác định có phải là có những nguyên nhân khác của viêm hoại tử gan, và điều quan trọng để làm như thế vì những nguyên nhân thông thường khác đáp ứng với các phương thức điều trị khác nhau. Trong tương lai, các chất phản ứng sinh học miễn dịch mới có thể đem lại lợi ích thêm cho bệnh nhân bị bệnh tự miễn.
Tóm tắt: Các ảnh hưởng đối với thực tiễn lâm sàng
■ Viêm gan tự miễn là một bệnh gan dạng viêm hoại tử chưa giải quyết được, đặc trưng bởi sự hủy hoại nhu mô gan.
■ Các dấu hiệu và triệu chứng của viêm gan tự miễn tương tự với các dấu hiệu và triệu chứng của các bệnh gan mạn tính khác.
■ Việc chẩn đoán viêm gan tự miễn thường được thực hiện sử dụng tiêu chuẩn mô tả. Tiêu chuẩn tính điểm có thể hữu ích đối với các trường hợp có thử thách về mặt chẩn đoán.
■ Nói chung, các kháng thể tự miễn (ví dụ ANA, SLA, kháng thể kháng LKM) không đặc hiệu đối với viêm gan tự miễn và mức độ biểu hiện của tự kháng thể có thể thay đổi đáng kể trong suốt tiến trình của bệnh.
■ Xơ gan mật nguyên phát (PBC) và viêm đường mật xơ chai nguyên phát (PSC) là các rối loạn ứ mật tự miễn có thể xảy ra cùng với viêm gan tự miễn hoặc bị nhầm lẫn với viêm gan tự miễn. Những tình trạng này có thể được phân biệt dựa vào biểu hiện của tự kháng thể, dựa vào mô học, và/hoặc chụp đường mật ngược dòng qua nội soi (ERC).
■ Hầu hết bệnh nhân bị viêm gan tự miễn đáp ứng với liệu pháp corticosteroid và/hoặc azathioprine.
■ Các thuốc ức chế miễn dịch thay thế có thể được thử nghiệm trên những bệnh nhân có đáp ứng dưới mức tối ưu đối với corticosteroid và azathioprine.
■ Nên xem xét ghép gan ở những bệnh nhân không cho thấy đáp ứng với liệu pháp ức chế miễn dịch.
■ Trong tương lai, các cách tiếp cận thay thế trong việc điều biến hệ miễn dịch có thể trở nên có sẵn.