 |
|
Xử lý các biến chứng của Xơ gan
I.Diễn tiến tự nhiên của Xơ gan
Có hai giai đoạn chính trong diễn tiến tự nhiên của xơ gan: xơ gan còn bù và xơ gan mất bù, được xác định theo các triệu chứng : có cổ trướng hoặc không có cổ trướng, xuất huyết do giãn tĩnh mạch, bệnh não gan có hoặc không có vàng da. Xơ gan còn bù và xơ gan mất bù là 2 thực thể riêng biệt với sự khác biệt về biểu hiện lâm sàng, các chỉ số tiên lượng, kết quả và tỷ lệ tử vong (Hình 1).
Hình 1. Lịch sử tự nhiên về bệnh gan mạn tính.

Hậu quả thường gặp nhất ở những bệnh nhân xơ gan còn bù là sự chuyển tiếp sang xơ gan mất bù, là một biến cố xảy ra ở khoảng 5% đến 7% bệnh nhân mỗi năm. Biến chứng dự đoán quan trọng nhất về sự mất bù là gradient áp lực tĩnh mạch gan (HVPG) > 10 mm Hg. Mức HVPG này được gọi là “tăng áp lực tĩnh mạch cửa có ý nghĩa lâm sàng”.
Đáng chú ý là ung thư biểu mô tế bào gan (HCC) có thể gây ra sự mất bù ở những bệnh nhân xơ gan còn bù và cũng là một biến dự đoán về tử vong ở xơ gan mất bù. Vì vậy, cần xem xét ung thư biểu mô tế bào gan như một chỉ số tiên lượng trong bất kỳ giai đoạn nào của bệnh hơn là một giai đoạn xơ gan khác biệt hoặc một biến cố xác định sự mất bù.
Phương tiện quan trọng nhất để dự đoán độ nặng và tử vong ở xơ gan mất bù là thang điểm Child-Turcott-Pugh (CTP) và thang điểm Mô hình bệnh gan giai đoạn cuối (MELD), sẽ được bàn luận chi tiết hơn trong tài liệu này. Gần đây hơn, 4 giai đoạn xơ gan khác nhau đã được xếp loại dựa trên dữ liệu về tỷ lệ tử vong sau 1 năm ở một nghiên cứu đoàn hệ lớn ở các bệnh nhân không được điều trị. 2 giai đoạn đầu tiên xảy ra ở xơ gan còn bù và được xác định theo sự không có giãn tĩnh mạch (giai đoạn 1) hoặc có giãn tĩnh mạch (giai đoạn 2). 2 giai đoạn khác xảy ra ở xơ gan mất bù và được xác định theo sự có cổ trướng (không có xuất huyết do giãn tĩnh mạch, giai đoạn 3) và xuất huyết do giãn tĩnh mạch (có hoặc không có cổ trướng, giai đoạn 4). Tỷ lệ tử vong sau 1 năm ở 4 giai đoạn này là 1%, 3%, 20% và 57% tương ứng.
Xử lý này tập trung vào việc xử trí các biến chứng của xơ gan, bao gồm xuất huyết do giãn tĩnh mạch, cổ trướng, hội chứng gan thận và bệnh não gan. Phương pháp sàng lọc để phát hiện ung thư biểu mô tế bào gan ở bệnh nhân xơ gan và các chỉ định cho việc ghép gan trong bệnh xơ gan cũng được bàn luận.
II.Xuất huyết do giãn tĩnh mạch
1.Xử trí không đặc hiệu xuất huyết do giãn tĩnh mạch cấp
Một trong những biến chứng chính liên quan với xuất huyết do giãn tĩnh mạch là nhiễm khuẩn. Việc dự phòng bằng kháng sinh ngắn hạn không chỉ làm giảm tỷ lệ nhiễm khuẩn mà còn làm tăng tỷ lệ sống còn và được xem là điều trị chuẩn. Mặc dù norfloxacin dạng uống được khuyến cáo do ý kiến đồng thuận, một thử nghiệm ngẫu nhiên có đối chứng mới đây đã cho thấy là ceftriaxone tiêm tĩnh mạch có thể là một lựa chọn tốt hơn ở bệnh nhân bị bệnh gan tiến triển và không ổn định về huyết động.
Ngoài việc dự phòng bằng kháng sinh, nên tăng thể tích máu qua truyền máu để duy trì huyết áp tâm thu 90-100 mm Hg và nhịp tim dưới 100 lần/phút. Mục tiêu của việc truyền máu là để duy trì nồng độ hemoglobin khoảng 8g/dL, việc thay thế máu toàn phần cũng nên giới hạn vì nếu nhiều quá cũng có thể liên quan với sự tái xuất huyết và tử vong thêm như đã được chứng minh ở các thử nghiệm có đối chứng sử dụng mô hình động vật.
Các nồng độ gradient áp lực tĩnh mạch gan > 20 mm Hg trong vòng 48 giờ của giai đoạn xuất huyết có liên quan với tăng tái xuất huyết và tỷ lệ tử vong. Một nghiên cứu thêm mới đây đã được thực hiện với trị liệu bằng thuốc có hoạt tính giãn mạch phối hợp với nội soi, sử dụng phân tích đa biến để phát triển 2 mô hình khác nhau có trị số tiên lượng tương tự. Một mô hình bao gồm HVPG > 20 mm Hg, huyết áp tâm thu < 100 mm Hg, và bệnh nguyên của bệnh gan không do rượu. Một mô hình khác thuần túy dựa trên các biến số lâm sàng và bao gồm điểm CTP, huyết áp tâm thu < 100 mm Hg, và bệnh nguyên của bệnh gan không do rượu. Những mô hình này có khả năng tương tự để dự đoán thất bại điều trị sau 5 ngày ở những bệnh nhân được điều trị bằng liệu pháp nội soi và dùng thuốc. Trong một nghiên cứu khác gồm những bệnh nhân có điểm MELD ≥ 18, là yêu cầu đối với hồng cầu khối ≥ 4 đơn vị trong 24 giờ đầu, và xuất huyết đang hoạt động qua nội soi có liên quan với tăng nguy cơ tử vong trong vòng 6 tuần.
2.Xử trí đặc hiệu xuất huyết do giãn tĩnh mạch cấp
Cơ sở sinh lý bệnh của việc điều trị giãn tĩnh mạch và xuất huyết do giãn tĩnh mạch được xem xét trong bảng sau:
Cơ chế tác dụng của các trị liệu khác nhau đối với giãn tĩnh mạch

* Mặc dù trên lý thuyết các nitrate tác động bằng cách làm giảm sự đề kháng, chúng thực sự tác động bằng cách làm giảm lưu lượng máu ở tĩnh mạch cửa qua việc giảm huyết áp động mạch trung bình.
Trong xuất huyết do giãn tĩnh mạch cấp, đã ghi nhận trị liệu bằng thuốc - các thuốc co mạch nội tạng đặc hiệu, phối hợp với trị liệu bằng nội soi có hiệu quả hơn từng điều trị đơn độc về mặt kiểm soát xuất huyết. Tuy nhiên, việc cộng thêm trị liệu bằng thuốc vào nội soi dường như không làm giảm đáng kể tỷ lệ tử vong. Trong số các thuốc co mạch an toàn có sẵn để điều trị xuất huyết do giãn tĩnh mạch cấp (somatostatin, terlipressin, vapreotide), hiện tại octrecotide là thuốc duy nhất được duyệt bởi Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA). Dữ liệu thuận lợi về độ an toàn của thuốc này cho phép bắt đầu điều trị trước khi dùng nội soi để chẩn đoán - tức là vào thời điểm chẩn đoán nghi ngờ ở phòng cấp cứu, và có thể tiếp tục điều trị trong 2-5 ngày sau khi có nguy cơ tái xuất huyết cao nhất.
Thắt búi giãn tĩnh mạch bằng nội soi (EVL) dường như hiệu quả hơn trị liệu gây xơ hóa tĩnh mạch bị giãn với sự kiểm soát nhiều hơn về xuất huyết, tỷ lệ tái xuất huyết giảm hơn và các biến chứng ít hơn mà không có sự khác biệt về tỷ lệ tử vong. Một nghiên cứu đã chọn ngẫu nhiên những bệnh nhân nghi ngờ bị xơ gan để điều trị gây xơ hóa (n = 89) hoặc thắt búi giãn tĩnh mạch bằng nội soi (n = 90) dưới dạng điều trị nội soi cấp cứu bổ sung vào trị liệu bằng somatostatin.. Thất bại trong điều trị xảy ra ở 21 bệnh nhân (24%) được điều trị bằng trị liệu gây xơ hóa so với 9 bệnh nhân (10%) được điều trị bằng thắt búi giãn tĩnh mạch bằng nội soi.
Tạo shunt cửa-chủ trong gan qua ngả tĩnh mạch cảnh (TIPS) vẫn được xem là một trị liệu cứu hộ trong việc kiểm soát xuất huyết cấp. Tuy nhiên, một thử nghiệm nhỏ ngẫu nhiên có đối chứng gồm 116 bệnh nhân xơ gan liên tục có xuất huyết do giãn tĩnh mạch cấp đã được điều trị một đợt tiêm xơ trong khi nội soi cấp cứu đã cho thấy là việc thiết lập sớm shunt cửa-chủ trong gan qua ngả tĩnh mạch cảnh (trong vòng 24 giờ bị xuất huyết) có liên quan với sự cải thiện đáng kể tỷ lệ sống còn ở những bệnh nhân có nguy cơ cao (tức là những người có HVPG > 20 mm Hg) và có thể có vai trò sớm hơn trong điều trị xuất huyết do giãn tĩnh mạch cấp.[16] Tuy nhiên những kết quả này cần có sự xác nhận ở những thử nghiệm lâm sàng lớn hơn đang được tiến hành.
Đã có báo cáo việc sử dụng tạm thời các stent kim loại có thể tự mở rộng để ngăn chặn xuất huyết do giãn tĩnh mạch cấp không kiểm soát được trong một nghiên cứu thí điểm ở 20 bệnh nhân cho thấy ngừng xuất huyết ở tất cả bệnh nhân mà không có biến chứng sau khi rút stent ra 2-14 ngày sau.
Đã có đề nghị về tác dụng có lợi của yếu tố VII được hoạt hóa tái tổ hợp (rFVIIa) ở những bệnh nhân Child-Turcott-Pugh (CTP) loại B và C bị xuất huyết do giãn tĩnh mạch cấp; tuy nhiên một thử nghiệm đa trung tâm, có đối chứng với giả dược mới đây được thực hiện trên nhóm bệnh nhân này đã cho thấy là việc dùng rFVIIa không có tác dụng có ý nghĩa thống kê về tiêu chí đánh giá tổng hợp (thất bại trong việc kiểm soát xuất huyết trong 24 giờ hoặc thất bại trong việc ngăn ngừa xuất huyết trở lại hoặc tử vong vào ngày thứ 5) so với giả dược (P = .37) hoặc về tỷ lệ tử vong sau 5 ngày. Các tác giả đã chỉ ra rằng mặc dù nhắm đến những bệnh nhân có nguy cơ cao, tỷ lệ thất bại ở nhóm giả dược thấp hơn nhiều so với dự kiến trong nghiên cứu này so với các thử nghiệm trước đây. Lưu ý là điều này có thể được giải thích một phần do sai lệch khi lựa chọn ở một số trung tâm tham gia, vì tính không đồng nhất ở tỷ lệ thất bại đã được ghi nhận ở các trung tâm khác nhau và các yếu tố chủ quan như thang điểm CTP đã được sử dụng làm tiêu chuẩn bao gồm vào phân tích. Các phát hiện từ nghiên cứu này đáng chú ý ở chỗ các bệnh nhân được điều trị với rFVIIa đã giảm tỷ lệ tử vong vào ngày thứ 42 và giảm tử vong liên quan với xuất huyết so với nhóm giả dược. Tuy nhiên, xét về toàn bộ, các kết quả của nghiên cứu này không hỗ trợ cho việc dùng thường xuyên rFVIIa trong trường hợp này.
3.Phòng ngừa tái phát giãn tĩnh mạch
Nhìn chung, các thử nghiệm về thắt búi giãn tĩnh mạch bằng nội soi (EVL) so với dùng phối hợp một thuốc chẹn beta không chọn lọc (NSBB) và isosorbide mononitrate đã cho thấy không có sự khác biệt có ý nghĩa thống kê về tỷ lệ tái xuất huyết hoặc tử vong rõ rệt trong trường hợp phòng ngừa tái phát giãn tĩnh mạch. Tuy nhiên, một thử nghiệm mới đây so sánh EVL cộng với trị liệu phối hợp thuốc (NSBB + isosorbide mononitrate) so với trị liệu phối hợp thuốc đơn thuần đã cho thấy tỷ lệ thấp hơn về tái xuất huyết do giãn tĩnh mạch ở nhóm dùng EVL cộng với trị liệu phối hợp thuốc (18% so với 34%) nhưng tỷ lệ chung về tái xuất huyết và tỷ lệ sống còn không khác nhau giữa các nhóm. Ngoài ra, 2 thử nghiệm khác ngẫu nhiên, có đối chứng, so sánh EVL đơn thuần so với EVL cộng với NSBB đã chứng minh lợi ích ở nhóm EVL cộng với NSBB, với tỷ lệ tái xuất huyết do giãn tĩnh mạch thấp hơn là 12% - 14% so với 29% - 38% khi dùng EVL đơn thuần. Sự phối hợp này hiện nay được khuyến cáo để phòng ngừa xuất huyết tái phát.
Điều quan trọng là những bệnh nhân đạt được sự giảm HVPG đến <12 mm Hg hoặc hơn 20% so với mức cơ bản có rất ít nguy cơ (~10%) tái xuất huyết do giãn tĩnh mạch, thấp hơn đáng kể so với những người không đáp ứng.Vì vậy, dường như hợp lý là các số đo HVPG sẽ hướng dẫn cho trị liệu này, mặc dù thủ thuật để đo HVPG cần có sự chuẩn hóa ở Mỹ. Việc đánh giá sự đáp ứng cần một lần đo HVPG thứ hai. 2 nghiên cứu mới đây cho thấy là đáp ứng tức thì của HVPG đối với các thuốc chẹn beta tiêm tĩnh mạch trong một thủ thuật duy nhất có thể dự đoán chính xác nguy cơ xuất huyết do giãn tĩnh mạch.
Mặc dù phương pháp tạo shunt cửa-chủ trong gan qua ngả tĩnh mạch cảnh (TIPS) được xem là trị liệu thứ 2 trong việc phòng ngừa tái xuất huyết, một thử nghiệm lớn đa trung tâm về TIPS so với tạo shunt lách (đầu xa)-thận đã cho thấy tỷ lệ tương tự về tái xuất huyết, bệnh não, và tử vong ở những bệnh nhân bị xơ gan CTP loại A/B đã thất bại khi trị liệu bằng thuốc/nội soi. Tuy nhiên, đã quan sát thấy một tỷ lệ cao rối loạn chức năng do shunt ở nhóm TIPS, có thể là việc sử dụng các stent TIPS trần.Vì vậy, ở những bệnh nhân thất bại với điều trị nội soi cộng với trị liệu bằng thuốc để phòng ngừa tái xuất huyết, có thể xem xét dùng TIPS có bao mặc dù tạo shunt bằng phẫu thuật cũng là một lựa chọn ở những bệnh nhân CTP loại A.
III.Cổ trướng
Trong xơ gan, cổ trướng là do 2 cơ chế bệnh sinh chính: tăng áp lực xoang và giữ natri (thứ phát do giãn mạch toàn thân và giãn mạch nội tạng) ( Hình 2). Một bệnh nhân bị xơ gan sẽ đi qua một trình tự gồm cổ trướng đáp ứng với thuốc lợi tiểu, tiếp theo là cổ trướng kháng trị, giảm natri huyết, và hội chứng gan thận (HRS), với mỗi giai đoạn phản ánh một tình trạng rối loạn tuần hoàn nhiều hơn.
Hình 2. Cơ chế sinh lý bệnh của sự hình thành cổ trướng và vị trí tác dụng của các trị liệu khác nhau.
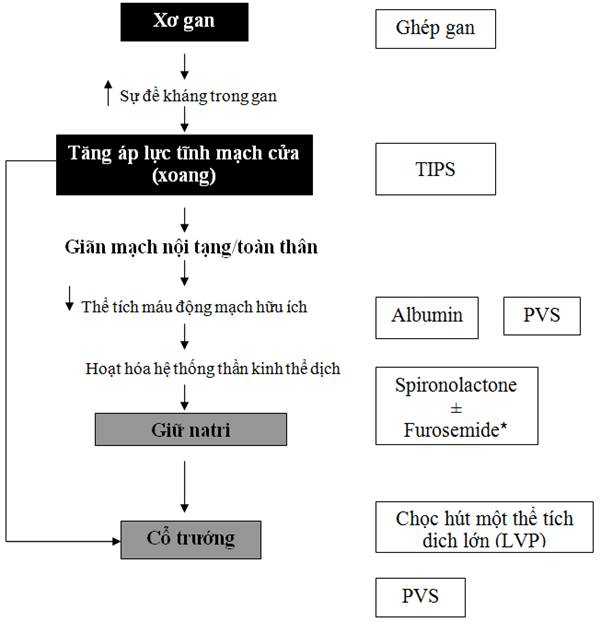
LVP: Chọc hút một thể tích dịch lớn; PVS: Tạo shunt tĩnh mạch màng bụng
* Chỉ nên dùng furosemide kết hợp với spironolactone.
1.Cổ trướng đáp ứng với thuốc lợi tiểu
Việc điều trị nhằm đạt được cân bằng natri âm tính (tức là hạn chế natri và dùng thuốc lợi tiểu) vẫn là nền tảng chính của điều trị. Ở những bệnh nhân bị cổ trướng căng, điều hợp lý là bắt đầu trị liệu bằng cách chọc hút một thể tích dịch lớn (LVP) để làm giảm khó chịu cho bệnh nhân, tiếp theo là điều trị bằng thuốc lợi tiểu. Có thể bắt đầu trị liệu bằng thuốc lợi tiểu với spironolactone đơn độc hoặc spironolactone cộng với furosemide. Cả hai cách tiếp cận đều có hiệu quả như nhau, tuy nhiên cần điều chỉnh liều thường xuyên hơn ở những bệnh nhân khởi đầu điều trị với trị liệu phối hợp. Ở nhóm bệnh nhân nội trú, các xét nghiệm có thể được theo dõi thường xuyên hơn thì có thể sử dụng trị liệu phối hợp. Tuy nhiên, ở nhóm bệnh nhân ngoại trú, khởi đầu đơn trị liệu bằng spironolactone được ưa thích hơn.
2.Cổ trướng kháng trị
Cổ trướng kháng trị được đặc trưng bởi sự thiếu đáp ứng đối với trị liệu lợi tiểu tối đa hoặc không thể khỏi được do bệnh nhân không thể dung nạp đủ liều thuốc lợi tiểu. Các trị liệu chính đối với cổ trướng kháng trị là chọc hút một thể tích dịch lớn (LVP) hàng loạt hoặc tạo shunt cửa-chủ trong gan qua ngả tĩnh mạch cảnh (TIPS). Một phân tích tổng hợp về 5 thử nghiệm ngẫu nhiên có đối chứng, so sánh những cách tiếp cận này cho thấy là TIPS tốt hơn đáng kể so với LVP trong việc kiểm soát cổ trướng kháng trị (tỷ số chênh [OR] về tái phát cổ trướng với TIPS so với LVP: 0,14, khoảng tin cậy [CI] 95%: 0,27-0,27). Ngoài ra, mặc dù tỷ lệ bệnh não cao hơn (tỷ số chênh: 2,26; khoảng tin cậy 95%: 1,35-3,76), TIPS có liên quan với xu hướng cải thiện tỷ lệ sống còn (tỷ số chênh: 0,74; khoảng tin cậy 95%: 0,40-1,37). Một phân tích tổng hợp sau đó về 4 thử nghiệm ngẫu nhiên có đối chứng bao gồm các dữ liệu của từng bệnh nhân đã cho thấy một tỷ lệ sống còn không ghép gan cao hơn có ý nghĩa thống kê ở nhóm TIPS so với nhóm LVP (P= .035). Ngược lại với những phát hiện này, 2 phân tích tổng hợp sớm hơn đã không cho thấy bất kỳ lợi ích về mặt sống còn nào liên quan với TIPS. Tuy nhiên, do nguy cơ bệnh não với TIPS, khởi đầu trị liệu bằng chọc hút một thể tích dịch lớn hàng loạt là một cách tiếp cận hợp lý.
Những bệnh nhân cần nhiều hơn 2-3 đợt chọc hút một thể tích dịch lớn mỗi tháng hoặc những người mà dịch cổ trướng khu trú thành khoang và không thể rút ra hết thì cần được đánh giá để dùng phương pháp TIPS. Mặc dù các nghiên cứu về việc dùng TIPS đối với cổ trướng kháng trị đã được thực hiện sử dụng các stent trần, nên sử dụng các stent có bao vì tỷ lệ rối loạn chức năng do shunt thấp hơn và khả năng nguy cơ về bệnh não và tử vong giảm hơn. Một theo dõi trong 2 năm bởi Bureau và cộng sự đã cho thấy tăng tỷ lệ thông suốt stent ở TIPS có bao so với TIPS không bao (76% so với 36%, tương ứng). Mặc dù mục tiêu của TIPS là làm giảm gradient áp lực ở hệ thống cửa-toàn thân xuống <12 mm Hg (ngưỡng để hình thành cổ trướng), việc giảm xuống đến các nồng độ quá thấp (ví dụ < 5 mmg Hg) đem lại nguy cơ cao hơn về bệnh não gan sau khi dùng phương pháp TIPS , vì vậy nên tránh.
Những bệnh nhân có bilirubin huyết thanh > 3 mg/dL, điểm CTP > 11, người già trên 70 tuổi, và/hoặc có dấu hiệu suy tim có nguy cơ tử vong cao hoặc có rối loạn chức năng do shunt không nên thực hiện phương pháp TIPS.Ở những bệnh nhân này, nên xem xét phương pháp tạo shunt tĩnh mạch màng bụng, đặc biệt vì mới đây một loạt trường hợp bệnh nhân trước khi ghép gan đã cho thấy là việc tạo shunt tĩnh mạch màng bụng không liên quan với các biến chứng thêm do phẫu thuật.
3.Trị liệu thực nghiệm đối với cổ trướng
Clonidin là một chất đồng vận alpha-2 tác dụng trên hệ thần kinh trung ương với hoạt tính ức chế giao cảm trong xơ gan. Trong một nghiên cứu thí điểm nhỏ, ngẫu nhiên, việc sử dụng clonidine cộng với spironolactone cho những bệnh nhân bị cổ trướng kháng trị đã làm tăng natri niệu và giảm đáng kể các nồng độ norepinepheine và aldosterone trong huyết tương cũng như hoạt tính của renin trong huyết tương. Ở một theo dõi trung bình 10,5 tháng, những bệnh nhân được điều trị bằng clonidine cộng với spironolactone (n=10) có tỷ lệ tái nhập viện vì cổ trướng ít hơn, thời gian tích tụ cổ trướng trở lại dài hơn, và giảm sự cần thiết dùng spironolactone so với những người đã được điều trị với LVP + albumin (n = 10). Một thử nghiệm ở một trung tâm, mù đôi, ngẫu nhiên, có đối chứng với giả dược do cùng những nhà nghiên cứu ở 64 bệnh nhân có cổ trướng “không biến chứng” và hệ thần kinh giao cảm được hoạt hóa (được xác định bởi nồng độ norepinephrine > 300 pg/mL) đã cho thấy số lượng bệnh nhân tái nhập viện vì cổ trướng thấp hơn đáng kể, thời gian tái nhập viện dài hơn, và sự cần thiết dùng LVP và thuốc lợi tiểu thấp hơn ở những bệnh nhân đang dùng clonidine so với những người đang dùng giả dược.
Các chất đối kháng thụ thể vasopressin type 2 (V2) cũng có tác dụng lợi niệu natri. Trong một nghiên cứu phase II ngẫu nhiên, mù đôi, có đối chứng với giả dược ở 148 bệnh nhân bị xơ gan cổ trướng không có giảm natri huyết, satavaptan đã dẫn đến tăng thể tích nước tiểu liên quan với liều dùng và giảm thể trọng mà không có các thay đổi về creatinine huyết thanh. Cũng vậy, một nghiên cứu ngẫu nhiên, mù đôi, có đối chứng với giả dược ở 151 bệnh nhân được điều trị bằng LVP cộng với spironolactone đã cho thấy là cộng thêm satavaptan có liên quan với thời gian tái phát cổ trướng cần LVP dài hơn và số lần chọc hút dịch thấp hơn so với số trường hợp quan sát được ở những bệnh nhân đang dùng giả dược.Vì vậy, dường như là các chất đối kháng thụ thể V2 có thể là thuốc bổ trợ hữu ích cho thuốc lợi tiểu trong việc điều trị cổ trướng bằng cách phòng ngừa giảm natri huyết do thuốc lợi tiểu và gây lợi tiểu natri hiệp đồng, mặc dù cần có sự phân tích thêm.
Giãn mạch là một trong những cơ chế chính trong bệnh sinh của cổ trướng (Hình 3). Một nghiên cứu thí điểm mới đây ở 39 bệnh nhân không có rối loạn chức năng thận trong đó 20 người có cổ trướng kháng trị đã cho thấy một liệu trình midodrine 7 ngày – là một chất co mạch alpha-adrenergic, có liên quan với tăng đáng kể natri niệu, tăng huyết áp động mạch trung bình ở tất cả bệnh nhân, và ở những bệnh nhân bị cổ trướng có liên quan với tăng độ thanh thải creatinine, giảm renin, và giảm aldosterone. Ngoài ra, một nghiên cứu nhỏ khác về những bệnh nhân bị cổ trướng kháng trị, một liệu trình midodrine 4 tuần làm giảm sự tích tụ cổ trướng.Tương tự, một nghiên cứu nhỏ trên những bệnh nhân có cổ trướng không kháng trị (n=15) và cổ trướng kháng trị (n=8) không có hội chứng gan thận (HRS) đã cho thấy là terlipressin làm tăng tỷ lệ lọc ở cầu thận và giảm natri niệu trong khi làm giảm hoạt tính norepinephine và renin trong huyết tương. Những kết quả này vẫn được xác định trong các thử nghiệm ngẫu nhiên lớn hơn.
4.Giảm natri huyết
Giảm natri huyết do hòa loãng chủ yếu được quy cho do suy giảm sự bài tiết nước tự do qua sự phóng thích vasopressin không thẩm thấu, là một biến chứng xảy ra ở những bệnh nhân bị xơ gan cổ trướng; trường hợp này thường không có triệu chứng vì nó phát triển chậm. Tuy nhiên, những dữ liệu mới đây cho thấy là giảm natri huyết là một yếu tố nguy cơ đối với sự phát triển bệnh não gan và nó dự đoán một chất lượng sống kém không phụ thuộc vào chức năng gan. Ngoài ra, những bệnh nhân sắp ghép gan có natri huyết thanh thấp nhạy cảm hơn với sự phát triển các biến chứng thần kinh, suy thận và nhiễm khuẩn trong tháng đầu sau khi ghép gan và còn giảm thời gian sống còn ngắn hạn (3 tháng) sau ghép gan. Giảm natri huyết còn là một yếu tố nguy cơ làm tăng tỷ lệ tử vong sau ghép gan. Do điều này, đã có đề nghị đưa natri vào hệ thống thang điểm Mô hình bệnh gan giai đoạn cuối (MELD).
Phương pháp xử trí giảm natri huyết thường được chấp nhận nhất là hạn chế dịch trong khoảng 1 - 1,5 lít/ngày, tuy nhiên, hiệu quả của phương pháp tiếp cận này còn giới hạn. Sự phóng thích vasopressin trong xơ gan do giảm thể tích máu động mạch hữu ích. Vì vậy, tăng thể tích huyết tương bằng albumin là một lựa chọn hợp lý. Trong một thử nghiệm nhỏ ngẫu nhiên có đối chứng, natri huyết thanh đã được cải thiện ở những bệnh nhân (n=12) được chọn ngẫu nhiên cho một liệu trình 7 ngày tiêm albumin tĩnh mạch (40 g/ngày) so với những bệnh nhân (n=12) được điều trị bằng cách hạn chế dịch chuẩn (1,5 lít ngày). Nồng độ natri huyết thanh tăng từ mức cơ bản 124 mmol/L lên 133 mmol/L vào ngày thứ 7 ở những bệnh nhân dùng albumin, trong khi các nồng độ tương đối không thay đổi đối với nhóm hạn chế dịch chuẩn. Ngoài ra, tỷ lệ phát sinh nhiễm khuẩn, bệnh não gan và tử vong khi nằm viện giảm ở nhóm được điều trị bằng albumin. Vì vậy, dường như là albumin có thể hữu ích khi dùng ngắn hạn, mặc dù dùng dài hạn dường như không thực tế và đắt tiền.
Một số thử nghiệm ngẫu nhiên có đối chứng cho thấy là các chất đối kháng thụ thể V2 là chất làm tăng tái hấp thu nước ở đoạn xa của ống thận, hữu ích trong việc cải thiện sự giảm natri huyết. Những thử nghiệm ngắn hạn về VPA-985 (lixivaptan) có đối chứng với giả dược đã cho thấy cải thiện natri huyết thanh phụ thuộc liều dùng với biến chứng chính là mất nước khi dùng liều cao nhất (250 mg, 2 lần/ngày). Tương tự, một thử nghiệm lớn đa trung tâm trong đó bệnh nhân được phân bổ ngẫu nhiên vào nhóm giả dược (n=223) hoặc tolvaptan dạng uống (n=225) với liều 15 mg/ngày đã cho thấy là tolvaptan được sử dụng trong 30 ngày ở bệnh nhân giảm natri huyết có thể tích máu lưu thông bình thường hoặc tăng thể tích (trong số 63 người bị xơ gan), có liên quan với sự cải thiện nhanh về natri huyết thanh và giảm cân đáng kể so với giả dược. Ngoài ra, không quan sát thấy tác dụng phụ hoặc rối loạn chức năng thận đáng kể.
Cuối cùng, các dữ liệu từ một thử nghiệm về satavaptan đa trung tâm đã cho thấy là dùng ngắn hạn trong 14 ngày ở những bệnh nhân bị xơ gan và giảm natri huyết đang dùng 100 mg spironolactone có hiệu quả trong việc điều chỉnh nồng độ natri huyết ở 2/3 bệnh nhân.Trong số 73 bệnh nhân tiếp tục dùng satavaptan trong 1 năm, nồng độ natri huyết thanh trung bình ở 47 bệnh nhân dùng satavaptan tăng từ 131-136 mEq/L vào tuần thứ 40, trong khi không có sự thay đổi về natri huyết thanh được xác định ở 26 bệnh nhân dùng giả dược, cho thấy là tác dụng của những thuốc này được duy trì trong một thời gian dài. Những thuốc này chưa được duyệt đối với bệnh nhân bị xơ gan cổ trướng. Một chất đối kháng thụ thể V1 –V2 là conivaptan được duyệt bởi FDA cho việc điều trị giảm natri huyết với thể tích máu lưu thông bình thường ở những bệnh nhân đã nhập viện. Tuy nhiên sự đối kháng thụ thể V1 có thể có một tác dụng có hại về huyết động trong xơ gan.
IV.Hội chứng gan thận
Suy thận cấp xảy ra ở 14% đến 25% bệnh nhân bị xơ gan nhập viện. Nguyên nhân thường gặp nhất là suy thận trước thận (chiếm 60% - 80% trường hợp), tiếp theo là hoại tử ống thận cấp (20% - 40%), với các nguyên nhân sau thận chiếm < 1% trường hợp (hình 3). Hội chứng gan thận (HRS) là một dạng suy thận trước thận vì do giãn mạch và giảm rõ rệt thể tích máu động mạch hữu ích dẫn đến co mạch thận. Điều này thường xảy ra ở những bệnh nhân bị cổ trướng kháng trị và/hoặc giảm natri huyết. HRS type 1 được đặc trưng bởi suy thận tiến triển nhanh chóng với nồng độ > 2,5 mg/dL hoặc giảm một nửa độ thanh thải creatinine đến 20 mL/phút sau một thời gian dưới 2 tuần. HRS type 1 đem đến tiên lượng kém, thường với tỷ lệ sống còn < 50% sau 1 tháng. HRS type 2 được đặc trưng bởi sự tăng từ từ về nồng độ creatinine huyết thanh đến > 1,5 mEq/dL, độ thanh thải creatinine < 40 mL/phút, hoặc natri niệu < 10 mEq/dL và trường hợp điển hình có liên quan với cổ trướng, không đáp ứng với thuốc lợi tiểu. HRS type 2 cũng đem đến tiên lượng kém dù tỷ lệ sống còn hơi lâu hơn một chút (tỷ lệ sống còn trung bình: ~6 tháng) trừ khi bệnh nhân được ghép gan.
Ở một bệnh nhân xơ gan bị hư hại đột ngột chức năng thận, một trong những bước đầu tiên là nên ngừng thuốc lợi tiểu và tăng thể tích nội mạch bằng albumin đường tĩnh mạch.Hai là, cần điều tra các yếu tố đã biết làm dễ bị suy thận trong xơ gan (nhiễm trùng, mất dịch hoặc mất máu, hạ huyết áp), và nếu có thì cần được điều trị. Tuy nhiên, thường khó phân biệt HRS với hoại tử ống thận cấp; các chỉ số nước tiểu bình thường, như độ thẩm thấu và natri có thể không hữu ích vì nồng độ natri niệu có thể thấp trong khi nhiễm trùng huyết và những quá trình khác có thể dẫn đến hoại tử ống thận. Vì vậy, sự xuất hiện HRS có thể bị che khuất do sự tăng nồng độ natri niệu, đặc biệt trong khi khởi phát hoại tử ống thận.
Hình 3. Cơ chế sinh lý bệnh đối với việc phát triển hội chứng gan thận

1.Trị liệu dứt điểm
Trị liệu dứt điểm đối với hội chứng gan thận (HRS) là ghép gan, vì đó là trị liệu duy nhất liên quan với thời gian sống còn lâu dài. Suy thận vào thời điểm ghép gan làm suy giảm kết quả ghép. Một nghiên cứu mới đây được tiến hành ở mô hình bệnh gan giai đoạn cuối (MELD) cho thấy suy thận trước khi phẫu thuật là một biến dự đoán độc lập về tỷ lệ sống còn trong ghép gan của người hiến tặng đã chết với nguy cơ tử vong tương đối ở các nhóm sau đây so với bệnh nhân có chức năng thận bình thường (creatinine = 0-0,99): 1) bệnh nhân có creatinine 1-1,99, nguy cơ tương đối 1,11; 2) bệnh nhân có creatinine > 2, nguy cơ tương đối 1,58, 3) bệnh nhân đang thẩm phân máu, nguy cơ tương đối 1,77; và 4) bệnh nhân cần ghép thận và gan, nguy cơ tương đối 1,44.
2.Cầu nối cho việc ghép gan
Vì quá trình gây hội chứng gan thận (HRS) là do giãn mạch toàn thân và nội tạng cực độ, các thuốc co mạch đã được dùng như một cầu nối cho việc ghép gan. Thuốc co mạch mạnh nhất đã được nghiên cứu là terlipressin. Một nghiên cứu nhỏ, biết rõ tên thuốc, có đối chứng với giả dược đã cho thấy là terlipressin có liên quan với sự cải thiện creatinine huyết thanh và tỷ lệ sống còn (n/N= 5/12 so với 0/12) so với giả dược; tuy nhiên, một thử nghiệm lớn mới đây, đa trung tâm, mù đôi, có đối chứng với giả dược về terlipressin so với giả dược trong điều trị HRS type 1 bao gồm 112 bệnh nhân đang dùng albumin đã cho thấy là mặc dù sự đảo ngược của HRS xảy ra có ý nghĩa thống kê, thường gặp hơn ở những bệnh nhân nhóm terlipressin (34% so với 12,5% tương ứng; P= .008), tỷ lệ sống còn không khác nhau có ý nghĩa thống kê giữa cả hai nhóm điều trị (43% so với 38% tương ứng). Đáng chú ý là tỷ lệ đảo ngược HRS 34% liên quan với việc điều trị bằng terlipressin thấp hơn nhiều so với tỷ lệ đã gặp ở các nghiên cứu không đối chứng. Tuy nhiên, nghiên cứu này cho thấy là tỷ lệ sống còn cải thiện có ý nghĩa thống kê ở những bệnh nhân đáp ứng với điều trị, bao gồm terlipressin, hỗ trợ cho các phát hiện tương tự từ những nghiên cứu khác sử dụng chất tương tự terlipressin. Một nghiên cứu khác mới đây biết rõ tên thuốc bao gồm 46 bệnh nhân có HRS cả type 1 và type 2 xác nhận hiệu quả của terlipressin, cho thấy sự cải thiện về chức năng thận có ý nghĩa thống kê với terlipressin cộng với albumin so với những bệnh nhân dùng albumin đơn độc (44% so với 9% tương ứng; P= .017), không có sự khác biệt về tỷ lệ sống còn 3 tháng.
Sự phối hợp midodrine và octreotide có hiệu quả ở 2 nghiên cứu nhỏ không đối chứng.Một nghiên cứu lớn hơn theo thời gian, hỗ trợ cho những phát hiện này và đã thấy sự cải thiện chức năng thận và giảm tỷ lệ tử vong ở 80 bệnh nhân được điều trị bằng midodrine cộng với octreotide đối với HRS so với các nhóm chứng. Dùng octreotide đơn độc cho thấy không có hiệu quả trong HRS khi so với giả dược hoặc với việc truyền vasopressin. Vì vậy, không chắc hiệu quả của trị liệu này là do dùng midodrine đơn độc hoặc phối hợp octreotide và midodrine. Các nghiên cứu thực nghiệm trên động vật cho thấy octreotide làm tăng tác dụng của các chất co mạch, gợi ý là sự phối hợp này được ưa thích hơn. Mặc dù vasopressin và dạng phối hợp noradrenaline dùng đường tĩnh mạch, - một chất đồng vận alpha-adrenergic khác, và albumin đã cho thấy có hiệu quả và an toàn trong các nghiên cứu nhỏ không có đối chứng, sự cần thiết đối với việc truyền những thuốc này ở một đơn vị hồi sức tích cực làm hạn chế khả năng áp dụng của chúng.
3.Các trị liệu đang được nghiên cứu
Một thử nghiệm mới đây đánh giá hiệu quả của phương pháp tạo shunt cửa-chủ trong gan qua ngả tĩnh mạch cảnh (TIPS) ở bệnh nhân HRS type I trước đây đã đáp ứng với octreotide/midodrine. Nghiên cứu này đã cho thấy là TIPS có liên quan với sự thành công lâu dài ở tất cả bệnh nhân với tăng tỷ lệ lọc ở cầu thận và bài tiết natri.Các nghiên cứu cũ hơn trong đó TIPS được dùng, bao gồm đa số bệnh nhân bị xơ gan do rượu, nhiều người đang nghiện rượu; vì vậy sự cải thiện quan sát được có thể là do cải thiện quá trình cấp tính trên bệnh mạn tính. Ngoài ra, tất cả nghiên cứu về TIPS đã loại trừ những bệnh nhân có điểm CTP ≥ 12. Với sự thiếu dữ liệu, chỉ nên dùng TIPS dưới dạng điều trị HRS type 1 trong các thử nghiệm theo thời gian ngẫu nhiên có đối chứng.
Trong một nghiên cứu nhỏ ngẫu nhiên có đối chứng, một phương pháp phân tích bổ sung sử dụng chất thẩm phân chứa albumin (thẩm phân albumin ngoài cơ thể) đã cho thấy cải thiện tỷ lệ sống còn 30 ngày ở 8 bệnh nhân có HRS type 1 so với 5 bệnh nhân được điều trị bằng lọc máu tĩnh mạch-tĩnh mạch ngắt quãng đơn độc. Các tác dụng có lợi rõ ràng trên huyết động toàn thân và trên bệnh não gan đã được quan sát thấy, tuy nhiên cần được bảo đảm ở các nghiên cứu thêm.
V.Viêm phúc mạc tự phát do vi khuẩn
Viêm phúc mạc tự phát do vi khuẩn (SBP) là một dạng nhiễm khuẩn thường gặp nhất ở những bệnh nhân xơ gan nhập viện, và sự nhận thức và điều trị sớm là phương tiện để cải thiện tỷ lệ sống còn ở những bệnh nhân này. Nghi ngờ trên lâm sàng về SBP cần được nêu lên khi bệnh nhân có các triệu chứng và/hoặc dấu hiệu trực tiếp do SBP, như sốt, đau bụng hoặc nhạy cảm đau, tăng bạch cầu, nhưng cũng cần nghi ngờ SBP khi có các biến chứng do nhiễm trùng huyết, như bệnh não không giải thích được, vàng da, và/hoặc suy thận nặng lên. Việc chẩn đoán SBP cần được thiết lập với đếm số lượng tế bào bạch cầu hạt > 250 tế bào/mm3, và nên bắt đầu điều trị trước khi có kết quả cấy vi khuẩn.
1.Điều trị các giai đoạn cấp của viêm phúc mạc tự phát do vi khuẩn (SBP)
Cephalosporin thế hệ thứ 3 (cefotaxime, ceftriaxone) là những thuốc lựa chọn trong điều trị viêm phúc mạc tự phát do vi khuẩn (SBP), mặc dù sự phối hợp amoxicillin và acid clavunic dường như có hiệu quả và an toàn như cefotaxime trong điều trị SBP. Nên tránh dùng các aminoglycoside ở bệnh nhân xơ gan vì sự liên quan của chúng với độc hại cho thận.
Rối loạn chức năng thận là nguyên nhân tử vong chính trong SBP và có thể được phòng ngừa bằng cách sử dụng albumin dùng đường tĩnh mạch. Các nghiên cứu đã xác nhận là rối loạn chức năng thận có nhiều khả năng xảy ra ở những bệnh nhân có bilirubin huyết thanh > 4 mg/dL, creatinine huyết thanh > 1 g/dL, hoặc nồng độ nitơ urê máu > 30 mg/dL lúc chẩn đoán, và việc sử dụng albumin trong SBP nên hạn chế đối với nhóm phụ bệnh nhân có nguy cơ cao này. Trong thực tế, một nghiên cứu mới đây đã cho thấy là những bệnh nhân có nguy cơ thấp về SBP (tức là những người có creatinine huyết thanh < 1 mg/dL và urê huyết thanh < 30 mg/dL), tiêu biểu cho khoảng một nửa số bệnh nhân bị SBP, có kết quả tốt mà không cải thiện với việc dùng albumin đường tĩnh mạch.
2.Phòng ngừa tái phát
Norfloxacin dùng hàng ngày có hiệu quả trong việc phòng ngừa tái phát viêm phúc mạc tự phát do vi khuẩn (SBP) và được xem là tiêu chuẩn thực hành.Việc sử dụng quinolone hàng tuần không được khuyến cáo vì nó đã cho thấy ít hiệu quả hơn so với norfloxacin dùng hàng ngày trong việc phòng ngừa tái phát SBP và có liên quan với một tỷ lệ cao hơn về phát triển các vi khuẩn kháng quinolone.
3.Các đối tượng cho điều trị dự phòng tiên phát
Một nghiên cứu mới đây có đối chứng với giả dược bao gồm những bệnh nhân nhập viện không có tiền sử viêm phúc mạc tự phát do vi khuẩn (SBP) với protein dịch cổ trướng (<1,5 g/L) là những người đã tiến triển suy gan (điểm CTP ≥ 9 và bilirubin huyết thanh ≥ 3 mg/dL) hoặc rối loạn chức năng thận (creatinine huyết thanh ≥ 1,2 mg/dL, nồng độ nitơ urê máu ≥ 25 mg/dl, hoặc nồng độ natri huyết thanh ≤ 130 mEq/L) đã cho thấy giảm xác suất bị SBP sau 1 năm (7% so với 61%), hội chứng gan thận (28% so với 41%), và tỷ lệ tử vong sau 3 tháng khi những bệnh nhân này được cho điều trị dự phòng tiên phát so với những người không điều trị dự phòng tương ứng. Đáng kể là dưới một nửa số bệnh nhân có protein dịch cổ trướng thấp đã đáp ứng với các tiêu chí đầu vào, và lợi ích về sự sống còn không kéo dài quá 1 năm. Một nghiên cứu khác có đối chứng với giả dược nhắm đến những bệnh nhân không có tiền sử SBP, với protein dịch cổ trướng thấp và nguy cơ thấp về phát triển SBP (bilirubin huyết thanh < 3,2 mg/dL, số lượng tiểu cầu > 98.000/tế bào/mm3) đã cho thấy xu hướng về tỷ lệ SBP thấp hơn (4% so với 14%, P= .07) và tỷ lệ tử vong thấp hơn (12% so với 28%, P= .04) ở những bệnh nhân được điều trị bằng ciprofloxacin dạng uống so với giả dược.
Tuy nhiên, tỷ lệ hiện mắc SBP rất thấp (0% - 3,5%) ở bệnh nhân xơ gan không có triệu chứng đang điều trị chọc hút dịch ngoại trú đối với cổ trướng kháng trị, vì vậy trừ khi những bệnh nhân này đáp ứng được các tiêu chí từ những nghiên cứu trước đây, họ không cần điều trị dự phòng bằng kháng sinh. Cần có các nghiên cứu thêm theo thời gian để xác định có phải xơ gan với nguy cơ thấp đối với SBP có thể có lợi do việc điều trị dự phòng tiên phát hay không.
VI.Bệnh não gan
Bệnh não gan (HE) là do tác dụng lên não của các chất thường được gan chuyển hóa. Mới đây bệnh não gan được xếp loại là theo chu kỳ (cấp tính trước đây), kéo dài (mạn tính trước đây), hoặc tối thiểu (dưới lâm sàng trước đây). Trong xơ gan, bệnh não gan là do sự kết hợp của shunt cửa-chủ và thất bại trong việc chuyển hóa các chất độc hại thận. Amoniac vẫn là chất độc hại thận quan trọng nhất trong sinh bệnh học của bệnh não gan; tuy nhiên, mặc dù nồng độ amoniac dường như có thể tương quan với độ nặng của bệnh não gan ở nhóm chứng, sự chồng chéo đáng kể về nồng độ amoniac toàn bộ theo cấp độ của bệnh não có thể xảy ra và những bệnh nhân không có bệnh não có thể thường có nồng độ amoniac bất thường. Vì vậy, không nên dùng nồng độ amoniac để chẩn đoán bệnh não gan và không cần theo dõi nồng độ này trong khi điều trị.
Hầu hết các trường hợp bệnh não gan là theo chu kỳ và có thể nhận dạng được yếu tố thúc đẩy. Trong những trường hợp này, cách tiếp cận chính là nhận dạng và xử lý yếu tố thúc đẩy, mặc dù có thể sử dụng trị liệu đặc hiệu ngắn hạn cho đến khi giải quyết được bệnh não gan kéo dài, trị liệu đặc hiệu nhằm để làm giảm sản xuất amoniac từ ruột qua việc dùng các disaccharide không hấp thu hoặc các kháng sinh không hấp thu.
Trước đây, chế độ ăn hạn chế protein được khuyến cáo trong bệnh não gan, nhưng các dữ liệu hỗ trợ cho khuyến cáo này không rõ. Ttrong một thử nghiệm duy nhất ngẫu nhiên có đối chứng tiến hành trên những bệnh nhân bị bệnh não gan theo chu kỳ, các kết quả giữa bệnh nhân theo chế độ ăn ít protein hoặc protein bình thường tương đương nhau. Sự hạn chế protein có thể đẩy mạnh sự thoái biến protein và nếu duy trì trong thời gian dài sẽ làm xấu đi tình trạng dinh dưỡng và làm giảm khối lượng cơ. Cơ xương có khả năng làm giảm amoniac máu bằng cách chuyển hóa amoniac thành glutamine; vì vậy nên tránh các biện pháp làm giảm khối lượng cơ ở bệnh nhân bị xơ gan. Các hướng dẫn mới đây từ các nhà nghiên cứu về lĩnh vực dinh dưỡng không còn khuyến cáo hạn chế protein nữa ở bất kỳ bệnh nhân nào bị bệnh não gan.
Các disaccharide không hấp thu được dùng đối với bệnh não gan là lactulose, lactitol, và lactose (ở những người không dung nạp lactose) và là trị liệu đầu tay được khuyến cáo hiện nay đối với bệnh não gan bởi Hiệp hội Tiêu hóa Mỹ.Một phân tích tổng hợp đánh giá các thử nghiệm về lactulose hoặc lactitol so với giả dược, kháng sinh hoặc không can thiệp đã cho thấy các disaccharide không hấp thu, so với giả dược hoặc không can thiệp có liên quan với xu hướng cải thiện các kết quả ở bệnh nhân bị bệnh não gan. Tuy nhiên, phân tích các thử nghiệm chất lượng cao không thấy có hiệu quả.Phân tích tổng hợp này đã cho thấy là các kháng sinh không hấp thu (neomycin, rifaximin) trội hơn các disaccharide không hấp thu trong việc cải thiện bệnh não gan, nhưng chưa rõ có phải những sự khác biệt này có liên quan về lâm sàng hay không. Đối với những bệnh nhân không dung nạp lactulose hoặc có các triệu chứng liên tục, kháng sinh thường được khuyến cáo như một lựa chọn điều trị thứ 2. Mới đây, đã có tăng sử dụng rifaximin vì dường như thuốc này an toàn hơn neomycin và cho thấy có hiệu quả như lactitol trong bệnh não gan theo chu kỳ,[98] nhưng thuốc tương đối đắt tiền. Trong một phân tích, đã thấy đơn trị liệu bằng rifaximin không có hiệu năng kinh tế trong điều trị bệnh não gan kéo dài, mặc dù chiến lược sử dụng rifaximin ở bệnh nhân kháng lại lactulose có thể có hiệu năng kinh tế cao.
Các trị liệu mới khác đối với bệnh não gan cần có sự nghiên cứu thêm là liệu pháp synbiotic (phối hợp probiotic và prebiotic) đã cho thấy cải thiện bệnh não gan tối thiểu, và thẩm phân albumin ngoài cơ thể (ECAD). Trong một thử nghiệm đa trung tâm, ngẫu nhiên có đối chứng, so sánh ECAD với trị liệu y khoa chuẩn ở bệnh nhân xơ gan nặng và bệnh não gan độ 3-4, ECAD có liên quan với sự cải thiện bệnh não gan sớm hơn và thường xuyên hơn.
VII.Hướng dẫn theo dõi Ung thư biểu mô tế bào gan (HCC) đối với bệnh nhân xơ gan
Theo dõi ung thư biểu mô tế bào gan (HCC) ở bệnh nhân xơ gan là thực tiễn thông thường trong nhiều năm. Mục đích của phương pháp sàng lọc là để nhận dạng các khối u ở giai đoạn đủ sớm khi chúng có thể dễ đáp ứng hơn đối với trị liệu chữa khỏi bệnh. Vì vậy, mục tiêu cuối cùng của việc theo dõi là để làm giảm tỷ lệ tử vong liên quan với HCC. Tuy nhiên, cho đến gần đây, tính hợp lý đối với việc sàng lọc giảm đi khi đã có phương pháp điều trị hiệu quả. Bruix và Sherman đã khuyến cáo là nên áp dụng việc theo dõi khi nguy cơ phát triển HCC vượt quá 1,5%/năm. Kết quả là tất cả bệnh nhân xơ gan được khuyến cáo sàng lọc HCC theo hướng dẫn thực tiễn của Hiệp hội Mỹ nghiên cứu về bệnh gan.
Chiến lược sàng lọc thường dùng nhất là thử nghiệm alpha-fetoprotein (AFP) trong huyết thanh và chụp siêu âm ở các khoảng cách 6 tháng hoặc 12 tháng. Khoảng cách này là dựa trên tỷ lệ phát sinh ung thư biểu mô tế bào gan (HCC) thấp ở những bệnh nhân có nguy cơ, điển hình là 1% - 4% mỗi năm, và sự phát triển chậm của những khối u này, với thời gian phát triển gấp đôi trung bình ước tính là 136 ngày. Khoảng cách và phương pháp sàng lọc tối ưu chưa được rõ và có thể thay đổi tùy theo chỉ định để sàng lọc. Tuy nhiên, không có sự khác biệt rõ rệt về tỷ lệ sống còn đối với những bệnh nhân được sàng lọc ở các khoảng cách 6 tháng hoặc 12 tháng. Hơn nữa, khoảng cách sàng lọc ngắn hơn thỉnh thoảng có thể phát hiện những khối u đã bị bỏ sót do độ nhạy hạn chế của các thử nghiệm hình ảnh (những khối u quá nhỏ không thể phát hiện được). Các khoảng cách ngắn hơn không thể được khuyến cáo cho tất cả bệnh nhân xơ gan nhưng được chỉ định khi nghi ngờ một khối u, ví dụ nồng độ AFP tăng lên dần hoặc một vùng nghi ngờ được nhận dạng trong một nghiên cứu hình ảnh trước đây.
Nồng độ AFP trong huyết thanh đã được sử dụng như một chất chỉ điểm của huyết thanh đối với ung thư biểu mô tế bào gan trong nhiều thập kỷ. Thử nghiệm này có tính đặc hiệu hạn chế do bệnh viêm mạn tính ở gan như viêm gan có thể làm tăng các nồng độ đến > 100 ng/mL. Tuy nhiên, một vấn đề hơn nữa là độ nhạy hạn chế của thử nghiệm ở mức 40% đến 60%.[105] Các chất chỉ điểm sinh học khác đang được đánh giá.
Cần nghi ngờ ung thư biểu mô tế bào gan khi đánh giá bất kỳ tổn thương gan cục bộ được phát hiện ở một bệnh nhân bị xơ gan. Khả năng chụp hình ảnh ổ bụng để phát hiện HCC đã được cải thiện đáng kể qua hai thập kỷ cuối, và các phương pháp được mô tả ở đây thường thay thế các thủ thuật xâm lấn nhiều hơn bao gồm chụp mạch máu, mở bụng thăm dò, và sinh thiết qua da là những phương pháp được ưa thích hơn để nhận dạng các khối u gan. Phương pháp chụp hình ảnh tùy thuộc vào một số yếu tố. Mặc dù chụp cắt lớp điện toán 3 pha và chụp cộng hưởng từ nhạy nhất, những phương pháp này đắt tiền và không thực tế cho việc sử dụng thông thường. Tuy nhiên, cần xem xét những phương pháp này khi siêu âm gặp khó khăn về kỹ thuật hoặc khi nhận dạng được một vùng nghi ngờ.
Nhiều trị liệu hiệu quả cao và ngay cả chữa khỏi bệnh đối với HCC hiện nay đã có, bao gồm cắt bỏ, ghép gan, và cắt bỏ tại chỗ. Việc áp dụng thích hợp các phương pháp can thiệp mang lại hy vọng kéo dài tỷ lệ sống còn đối với nhiều bệnh nhân có biến chứng khác của bệnh gan gây tử vong này.
VIII.Các chỉ định cho việc ghép gan
Sự phát triển mất bù (cổ trướng, xuất huyết do giãn tĩnh mạch, bệnh não gan) ở những bệnh nhân xơ gan có liên quan với tỷ lệ sống còn trung bình chỉ 1,5 năm ,vì vậy nên xem xét ghép gan ở những bệnh nhân này. Điểm CTP được nêu ra sớm dựa trên 5 thông số: bệnh não, cổ trướng, bilirubin, albumin, và thời gian prothrombin. Điểm CTP đã được sử dụng trong nhiều năm để đánh giá tiên lượng của xơ gan và là một biến dự đoán quan trọng về tử vong cả xơ gan còn bù và xơ gan mất bù. Tuy nhiên, điểm CTP có những hạn chế quan trọng, chủ yếu là do sự diễn dịch chủ quan về một số trong các thông số của nó.
Điểm MELD, được thiết kế độc đáo để đánh giá tiên lượng của bệnh nhân xơ gan đang dùng phương pháp TIPS, là một điểm số liên tục dựa trên 3 biến số khách quan: creatinine, tỷ lệ chuẩn hóa quốc tế thời gian prothrombin, và bilirubin. Điểm MELD cho thấy dự đoán chính xác tỷ lệ tử vong 3 tháng trong số những bệnh nhân bị xơ gan ở trong danh sách chờ được ghép gan và hiện nay được sử dụng có hiệu quả ở Mỹ để phân bổ gan của người hiến tặng đã chết.
Tuy nhiên, MELD không phải là một chỉ điểm tiên lượng toàn thể về xơ gan, và một số ngoại lệ của MELD cần có các phương pháp tiếp cận đặc hiệu thêm. Tử vong trước khi ghép gan vẫn thường gặp, và nhiều trường hợp tử vong xảy ra sớm mặc dù điểm MELD thấp lúc khởi đầu. Ở những bệnh nhân có điểm MELD < 21, natri huyết thanh thấp và cổ trướng dai dẳng được thấy là các biến độc lập về tỷ lệ tử vong. Một số nghiên cứu khác đã xác nhận trị số về giảm natri huyết là một chỉ số tiên lượng bổ sung ; tuy nhiên, việc sử dụng chỉ điểm này phức tạp do sự kiện là nó có thể bị thay đổi do việc sử dụng các thuốc lợi tiểu, các dung dịch dùng đường tĩnh mạch, và/hoặc các chất đối kháng thụ thể V2. Sự có mặt của HCC trong tiêu chuẩn Milan (khối u đơn độc < 5 cm hoặc tối đa 3 khối u, mỗi khối u < 3 cm) cho phép chỉ định dùng MELD thêm, và vì vậy nên kể đến những bệnh nhân này để ghép gan.
Tình trạng huyết động xấu thêm ở bệnh nhân xơ gan như sự xuất hiện hội chứng não gan (HRS), cũng được thấy là một chỉ số tiên lượng. Trong một nghiên cứu mới đây nhằm đánh giá các yếu tố tiên lượng trong hội chứng gan thận (HRS), điểm MELD và loại HRS (loại 1 hoặc 2) là các biến độc lập về tỷ lệ tử vong. Mặc dù tất cả bệnh nhân bị HRS type 1 có điểm MELD cao (>20) và có kết quả rất kém (tỷ lệ sống còn trung bình: 1 tháng), tỷ lệ sống còn của những bệnh nhân bị HRS type 2 thì lâu hơn và phụ thuộc vào điểm MELD. Những dữ liệu này cho thấy là sự phát triển HRS type 1 tự bản thân nó thể hiện một sự ưu tiên cao đối với việc ghép gan, không phụ thuộc vào điểm MELD.
Các biến chứng đặc hiệu khác của xơ gan có thể bị đánh giá thấp bởi điểm MELD là bệnh gan mạn tính, tràn dịch màng phổi do gan, hội chứng gan phổi, và tăng áp cửa-phổi. Những tình trạng này có thể xảy ra ở những bệnh nhân có điểm MELD thấp nhưng có tỷ lệ tử vong cao trong trường hợp có ghép gan. Điểm MELD không phải là một chỉ điểm tiên lượng toàn thể của xơ gan, và việc điều chỉnh hoặc cộng thêm các biến số bổ sung sẽ cần thiết để xử trí một số vấn đề đặc hiệu.
IX.Kết luận
Xơ gan tiêu biểu cho giai đoạn cuối của bất kỳ bệnh gan mạn tính nào và có thể vẫn còn bù trong nhiều năm trước khi phát triển một biến cố mất bù. Xơ gan mất bù được biểu thị bằng sự phát triển bất kỳ hoặc tất cả các biến chứng sau đây: Xuất huyết do giãn tĩnh mạch, bệnh đông máu, cổ trướng, viêm phúc mạc tự phát do vi khuẩn, hội chứng gan thận, giảm natri huyết, giảm albumin huyết, và/hoặc bệnh não gan. Do tiên lượng bệnh kém, trị liệu có hiệu quả duy nhất đối với xơ gan mất bù là ghép gan.
Tóm tắt: Các ảnh hưởng đối với thực tiễn lâm sàng