 |
|
chiến thuật điều trị viêm gan b mạn
chọn lựa thuốc gì? khi nào thay đổi điều trị? khi nào ngưng điều trị?
I.GIỚI THIỆU:
Đã có những tiến bộ lớn về bệnh viêm gan B từ các nghiên cứu gần đây về diễn tiến tự nhiên của bệnh cũng như từ các thử nghiệm lâm sàng của các thuốc kháng virus. REVEAL, một nghiên cứu dài hơn một thập niên về vài ngàn bệnh nhân viêm gan virus B với kháng nguyên bề mặt (HBsAg) dương tính ở người trưởng thành Đài Loan, đã chứng minh rằng mức độ HBV DNA ban đầu ở những người mang HBsAg trong độ tuổi từ 30-65 tuổi có liên quan trực tiếp đến khả năng phát triển ung thư biểu mô tế bào gan nguyên phát và xơ gan 10 năm sau. Các nghiên cứu khác đã đi đến kết luận tương tự . Về vấn đề điều trị, nó đã được chứng minh rằng ức chế virus lâu dài làm giảm tỷ lệ các kết cục xấu lâm sàng , đặc biệt là ở bệnh nhân xơ hóa tiến triển . Điều quan trọng chắc chắn cho rằng việc tiếp tục ức chế virus vẫn có lợi cho dù sự xuất hiện đề kháng làm giảm giá trị điều trị.
Những nghiên cứu diễn tiến tự nhiên và điều trị lâm sàng này đã dẫn đến xuất hiện một khái niệm đơn giản nhưng sâu sắc là "hai vấn đề song hành " của điều trị viêm gan B : sự sử dụng lâu dài thuốc ức chế virus và việc tránh xuất hiện đề kháng. Nguyên lý phù hợp là với sự ức chế virus hoàn toàn tạo nên lợi ích lâm sang tối đa, và lượng virus trong máu còn sót lại tại các thời điểm trong khi điều trị với một số thuốc chống virs bằng đường uống đã được chứng minh làm tăng nguy cơ đề kháng với điều trị, và điều này có khả năng ảnh hưởng đến kết quả bệnh nhân .
Các trang bị y tế điều trị phát triển đối với virus viêm gan B (HBV) khiến nó ngày càng tốt để đạt được mục tiêu kép là ức chế virus lâu dài và tránh sự đề kháng trong phần lớn các bệnh nhân. Tính sẵn có hiện tại của 4 chất tương tự nucleos(t)ide, với những chất khác, cùng với interferon tiêu chuẩn và peginterferon, cung cấp cho các bác sĩ lâm sàng nhiều tùy chọn điều trị cho bệnh nhân của họ. Tuy nhiên, khoảng rộng các lựa chọn điều trị này tạo ra thách thức đối với bác sĩ lâm sang, người phải lựa chọn thuốc điều trị thích hợp điều trị cho bệnh nhân mà việc điều trị được chỉ định. Quyết định điều trị ban đầu liên quan đến sự lựa chọn giữa một chế độ interferon alfa chuẩn đã được công nhận hoặc thuốc bằng đường uống được chấp thuận. Nếu một loại thuốc uống được chọn, các câu hỏi khác theo sau, chẳng hạn như có thuốc được dùng và liệu sự kết hợp trị liệu có thể đem lại bất kỳ lợi ích bổ sung nào không.
Quyết định đối với điều trị ban đầu là không tránh khỏi bị ràng buộc với câu hỏi rằng liệu điều trị có thể ngừng lại không và nếu có thì khi nào. Câu trả lời yêu cầu việc xem xét mục tiêu điều trị mong muốn đã đạt được không và, điều quan trọng tương đương là mục tiêu này và những lợi ích lâm sàng liên quan với nó có thể được duy trì không nếu việc điều trị được ngừng lại. Ngoài ra, quản lý bệnh nhân điều trị viêm gan B nên được coi là một quá trình động của việc đánh giá liên tục các thông số đáp ứng để đảm bảo đạt được tối ưu mục tiêu kép của ức chế virus lâu dài và tránh đề kháng. Những công bố gần đây đã cố gắng thiết lập những mốc điều trị tại một số thời điểm quan trọng trong quá trình điều trị, trong trường hợp không đạt được tiêu chuẩn đó, quyết định những thay đổi chủ động trong điều trị. Các chỉ số của đáp ứng khác nhau đối với các thuốc kháng virus khác nhau như chức năng các đặc tính: hàng rào di truyền cho đến đề kháng.
Điều này chỉ ra các câu hỏi: thuốc nào được lựa chọn, khi nào thực hiện thay đổi trong điều trị, và khi nào ngừng điều trị ở những bệnh nhân đã được lựa chọn cho điều trị HBV. Nhiều sự tranh cãi kéo dài đối với câu hỏi ở những bệnh nhân nào trong điều trị, đó là một chủ đề quan trọng được thực hiện bởi Anna SF Lok, MD, trong "Điều trị viêm gan B mãn tính: Ai sẽ điều trị và Khi nào điều trị?
II.CHỌN ĐIỀU TRỊ NÀO?
Thách thức đầu tiên cần đối mặt của một người lâm sang, người lập kế hoạch để điều trị một bệnh nhân viêm gan B mãn là thuốc nào được lựa chọn. Các thuốc được công nhận tại Hoa Kỳ cho HBV có thể được phân thành 2 nhóm, điều trị interferon alfa chuẩn và điều trị bằng các nucleos(t)ide uống như bên dưới:
A.Điều trị Interferon alfa chuẩn
Mặc dù interferon alfa-2b đã được chấp thuận cho điều trị viêm gan B vào năm 1991 , nhưng tại thời điểm hiện nay tại Hoa Kỳ, việc điều trị interferon được ưa chuộng là peginterferon alfa-2a vì tiện lợi sử dụng. Peginterferon alfa-2a được chấp thuận cho điều trị viêm gan B ở liều 180 μg / tuần trong 1 năm, dựa trên 2 nghiên cứu chủ chốt . Ở những bệnh nhân HBeAg dương tính, điều trị bằng interferon có thể được mong muốn đem lại sự chuyển đổi huyết thanh HBeAg trong khoảng 30% các cá nhân sau 1 năm điều trị - một tỷ lệ cao hơn đáng kể so với 12% đến 23% được thấy với 1 năm điều trị bằng thuốc uống. Chống lại lợi thế này, tuy nhiên, là tỉ lệ gia tăng được tích lũy của chuyển đảo ngược HBeAg huyết thanh với điều trị kéo dài thuốc uống (các tỉ lệ tăng đến ~ 30% sau 2 năm điều trị và hơn 40% sau 3 năm điều trị. Thậm chí giả định rằng việc sử dụng kéo dài hơn interferon sẽ dẫn tới tỷ lệ đáp ứng cao hơn, quá trình dùng nó và các triệu chứng bất lợi làm cho việc sử dụng duy trì nó dài hơn 1 năm có vấn đề. Do đó, các bác sĩ lâm sàng có thể kết luận hợp lý rằng tốt hơn là sử dụng điều trị bằng đường uống trong 2-3 năm, hoặc thậm chí lâu hơn, hoặc interferon trong 1 năm.
Một ưu điểm được coi là ưu thế của interferon là khả năng đạt được mục tiêu mất HBsAg hoặc chuyển đổi huyết thanh HBsAg trong 3% đến 8% của những bệnh nhân có kháng nguyên e viêm gan B (HBeAg) dương tính sau 1 năm điều trị. Mất HBsAg đã được quan sát với việc dùng thuốc uống là ≤ 1% ở hầu hết các nghiên cứu của adefovir, lamivudine, và telbivudine. Entecavir xuất hiện tạo ra tỉ lệ cao hơn của việc HBsAg mất (2 %) ở bệnh nhân HBeAg dương tính sau 1 năm điều trị. Tuy nhiên, tỷ lệ bệnh nhân HBeAg dương tính mất HBsAg là 5% và 3% sau 2 năm điều trị với entecavir hoặc lamivudine, riêng từng chất tương ứng. Hơn nữa, trong một thử nghiệm quan trọng gần đây của tenofovir ở những bệnh nhân HBeAg dương tính, 3% mất HBsAg sau 1 năm điều trị. Do đó, mặc dù interferon có thể vẫn giữ lại một ưu thế trong việc đạt được HBsAg mất sau 1 năm điều trị, nhưng nó không còn được xem là khả năng duy nhất để đạt được đích cuối này.
Ở bệnh nhân HBeAg-âm tính, từ lâu đã nhận ra rằng điều trị bằng interferon alfa chuẩn cũng có thể ức chế số lượng HBV DNA, nhưng tồn tại một rủi ro tái phát chắc chắn sau khi ngưng điều trị. Điều này có thể được giảm bớt với việc sử dụng kéo dài alfa interferon (ví dụ, lên đến 2 năm), nhưng nhiều bác sĩ lâm sàng có thể xem vấn đề này là quá dài để điều trị được chấp nhận ở hầu hết bệnh nhân. Tuy nhiên, ngay cả 1 năm dùng peginterferon alfa-2a liên quan đến một tỉ lâu bền cao hơn về việc ức chế virus sau một đợt điều trị tự giới hạn so với khả năng có thể đạt được với 1 năm điều trị thuốc uống. Ngưỡng HBV DNA không phát hiện được quan sát thấy trong gần 20% các bệnh nhân tại thời điểm 4 năm sau khi ngừng điều trị peginterferon alfa. Mặc dù có dữ liệu cho thấy rằng việc kéo dài điều trị bằng đường uống có thể dẫn đến duy trì ức chế virus sau khi điều trị đã ngừng lại, đối với hầu hết các bác sĩ lâm sàng hiện nay việc quyết định điều trị ban đầu bằng đường uống ở một bệnh nhân HBeAg-âm tính là tương tự như quyết định để việc điều trị là vô thời hạn. Vì lý do này, peginterferon alfa-2a được ưa chuộng bởi một số chuyên gia cho điều trị đầu tiên ở bệnh nhân HBeAg-âm tính, và nó vẫn là một trong các tùy chọn khuyến khích cho lần đầu điều trị trong cả hai nhóm bệnh nhân HBeAg dương tính và HBeAg âm tính ở những hướng dẫn điều trị bệnh gan của Hiệp hội Mỹ (AASLD: The American Association for the Study of Liver Diseases).
B.Điều trị các Nucleos(t)ide bằng đường uống
Mặc dù dữ liệu chính xác còn thiếu, phần lớn các bệnh nhân được nhận điều trị do FDA (Food and Dryg Adminitration) Hoa Kỳ chấp thuận cho viêm gan B mãn tính tại Hoa Kỳ được điều trị bằng các nucleos(t)ide vì tính hiệu quả và khả năng dung nạp tốt của chúng.
1.Lamivudine. Sự ra đời của lamivudine vào cuối những năm 1990 là một cuộc cách mạng vào thời điểm đó: đó là thuốc uống đầu tiên được công nhận để điều trị viêm gan B mãn tính, và nó vẫn còn được sử dụng rộng rãi trên thế giới. Tuy nhiên, lamivudine có đề kháng xấu, với 23% bệnh nhân đề kháng tại domain YMDD của DNA polymerase (codon rtM204V/I/S) tại năm đầu tiên điều trị, tăng tới 46% tại năm 2, 55% ở năm 3, và sau đó 65-71% ở năm 4 và 5 . Hơn nữa, hầu hết các cá nhân này sẽ phát triển thêm 1 hoặc nhiều đột biến nữa ở codon rtV173L và / hoặc rtL180M, vị trí bảo quản sự tái tạo của virus. Với những hiện tượng này, lamivudine không còn được sử dụng như một loại thuốc đầu tiên trong viêm gan B mãn tính khi các lựa chọn khác có khả năng, như đã được thể hiện trong hướng dẫn điều trị gần đây.
2.Adefovir. Adefovir, một chất tương tự nucleotide, là thuốc uống thứ hai được giới thiệu cho bệnh viêm gan B mạn. Mặc dù hoạt tính kháng virus của adefovir và thông tin kháng thuốc được cải thiện so với lamivudine, nhưng thuốc này đã không đem lại một tỉ lệ ức chế virus lớn hơn lamivudine với liều 10 mg được đề nghị hàng ngày để tránh độc thận, ở liều cao adefovir hơn được quan sát trong các thử nghiệm HIV trước đó. Trong những cuộc thử nghiệm quan trọng, HBV DNA âm tính lúc 1 năm đạt được 21% và 51% ở bệnh nhân HBeAg dương tính và HBeAg âm tính. Chuyển đổi huyết thanh HBeAg xảy ra ở 12% bệnh nhân sau 1 năm, nhưng tỷ lệ dần dần tăng lên 48% sau 5 năm. Adefovir có một lý lịch đề kháng tốt hơn nhiều so với lamivudine, với tỉ lệ đề kháng cộng dồn genotypic là 0% và 3% ở 1 và 2 năm, mặc dù tỷ lệ đề kháng genotypic đã tăng đến 29% trong nghiên cứu mở rộng 5-năm quan trọng được thực hiện ở bệnh nhân HBeAg-âm tính. Tuy nhiên, ở bệnh nhân có HBV DNA <1.000 copies/ ml ở năm đầu tiên thì tỷ lệ đề kháng tại năm 4 chỉ là 4%.
3.Entecavir. Entecavir đã được phê duyệt tại Hoa Kỳ vào năm 2005. Trong những nghiên cứu chủ chốt trong 1 năm, entecavir 0,5 mg hàng ngày ức chế HBV DNA đến mức không thể phát hiện ở 67% những trường hợp HBeAg dương tính và 90% bệnh nhân HBeAg-âm tính so với 36% và 72% tương ứng với từng nhóm khi dùng lamivudine. Tuy nhiên, cũng như tất cả các thuốc kháng virus uống được nghiên cứu cho đến nay, hiệu quả kháng virus lớn hơn đã không dịch chuyển được tỷ lệ chuyển đổi huyết thanh HBeAg cao hơn: 21% với entecavir và 18% với lamivudine. Cũng tương tự như các nghiên cứu trước đó với các các thuốc khác, sự duy trì ức chế virus là hiếm khi được thấy ở bệnh nhân HBeAg-âm tính những người đã ngừng điều trị sau 1 năm. Quan sát kéo dài ở các bệnh nhân HBeAg dương tính từ chương trình này cho thấy một tỷ lệ cộng dồn sự sạch HBV DNA ở hơn 90% trường hợp sau 4 năm. Lưu ý rằng các bệnh nhân nhận entecavir dài hạn vì không đáp ứng ban đầu , thất bại đối với việc làm sạch HBeAg, hoặc tái phát sau khi sạch HBeAg trong năm đầu tiên đã được dùng một liều entecavir dài hạn 1,0 mg / hàng ngày.
Các dữ liệu đề kháng của entecavir đã được chứng minh là rất tốt, với tỷ lệ cộng dồn đề kháng genotypic là 1,2% tại thời điểm 5 năm ở những bệnh nhân tự nguyện nhận điều trị trước đó. Các hàng rào di truyền cao đối với đề kháng của entecavir ở những bệnh nhân điều trị tự nguyện có thể giải thích vì quy luật của những đột biến thay thế 3 amino acid trong DNA polymerase do đề kháng xảy ra, bao gồm 2 trong những đột biến liên quan đến đề kháng của lamivudine (ví dụ: M204V / I + L180M) cộng với một đột biến liên quan đến entecavir “được ký hiệu bổ sung” tại locus 169 , 202 hoặc 250. Trái ngược hoàn toàn, ở những bệnh nhân đề kháng lamivudine, khoảng 35% bệnh nhân xuất hiện đề kháng entecavir 1,0 mg dùng hàng ngày trong vòng 3 năm khi được chuyển sang dùng entecavir. Vì thế, đơn trị liệu với entecavir bây giờ phải được coi là một lựa chọn gần tốt nhất cho bệnh nhân đề kháng lamivudine, và phương thức cho việc điều trị những bệnh nhân đề kháng lamivudine đã dứt khoát thay đổi theo hướng bổ sung thêm, như một chất tương tự nucleotide: adefovir hoặc tenofovir.
4.Telbivudine. Được phê duyệt vào năm 2006 với liều 600 mg mỗi ngày, đây là một chất ưu việc với lợi điểm đã được chứng minh so với lamivudine trong các thử nghiệm trọng yếu. Sau 1 năm điều trị, HBV DNA không phát hiện được ở 60% số HBeAg dương tính và 88% bệnh nhân HBeAg-âm tính. Chuyển đổi huyết thanh HBeAg xảy ra ở 23% người nhận telbivudine ở 1 năm so với 21% người nhận lamivudine. Tỷ lệ cộng dồn chuyển đổi HBeAg huyết thanh ở năm 2 với telbivudine là 31% so với 26% với lamivudine.
Các dữ liệu đề kháng của telbivudine thì tốt hơn của lamivudine, nhưng vẫn có một nguy cơ đề kháng 5% và 2% sau 1 năm ở những bệnh nhân HBeAg dương tính và những bệnh nhân HBeAg âm tính, tương ứng với từng nhóm, với mức đề kháng cao hơn là 25% và 11% quan sát được tại tuần lễ 104. Thông tin từ thử nghiệm quan trọng của việc dùng telbivudine để chứng minh mối quan hệ giữa việc ức chế virus trong quá trình điều trị và tỷ lệ ức chế virus duy trì, chuyển đổi huyết thanh HBeAg, và đề kháng. Việc ức chế virus hoàn toàn ở tuần 24 có liên quan với kết quả vượt trội về tất cả các chỉ số được quan sát. Đáng chú ý nhất, tỷ lệ đề kháng tại tuần 92 là 4% ở bệnh nhân HBeAg dương tính và 2% ở bệnh nhân HBeAg âm tính nếu họ đã không thể phát hiện HBV DNA ở tuần 24. Ngược lại, 30% đến 60% ở cả hai những bệnh nhân HBeAg dương tính và HBeAg âm tính được phát hiện đề kháng telbivudine sau 92 tuần nếu họ đã có HBV DNA trên 4 log10 copies/ mL lúc 24 tuần, với tỉ lệ đề kháng trung bình cho các bệnh nhân có mức độ còn virus trong máu thấp hơn tại Tuần 24. Trong một phân tích gần đây của nghiên cứu GLOBE, Zeuzem và các đồng nghiệp thấy rằng trong các nhóm nhỏ bệnh nhân HBeAg-dương tính với HBV DNA lúc ban đầu dưới 109 copies/mL và ALT gấp 2 lần giới hạn trên của bình thường, sự đề kháng với telbivudine xuất hiện tại thời điểm 2 năm chỉ trong 1,8% bệnh nhân miễn là họ đạt được HBV DNA không thể phát hiện tại tuần 24. Tương tự, trong tập hợp con của bệnh nhân HBeAg-âm tính với HBV DNA lúc ban đầu dưới 107 copies/mL là những người đạt HBV DNA được không thể phát hiện ở 24 tuần là 2% xuất hiện đề kháng ở năm 2.
5.Tenofovir. Tenofovir tương tự acyclic nucleotide, khác với adefovir ở 1 nhóm methyl, đã được chấp thuận để điều trị HIV năm 2002 và có hoạt tính chống HBV ở dân số đồng nhiễm HIV/ HBV cũng như trong ống nghiệm. Những báo cáo về hàng loạt các trường hợp, trong đó tenofovir được sử dụng ở bệnh nhân chỉ nhiễm HBV cũng chỉ ra hoạt tính đáng kể đối với HBV. Những dữ liệu gần đây từ những thử nghiệm so sánh ngẫu nhiên lớn quan trọng đã được trình bày tại Hội nghị AASLD thường niên năm 2007 xác nhận rằng tenofovir 300 mg dùng hàng ngày thì liên quan với những tỉ lệ ấn tượng về ức chế virus tại 48 tuần điều trị ở những bệnh nhân đơn nhiễm HBV. Trong những nghiên cứu này, 76% bệnh nhân HBeAg dương tính và 93% bệnh nhân HBeAg âm tính thì đạt được HBV DNA âm tính bằng PCR phân tích sau 48 tuần điều trị tenofovir so sánh với chỉ 13% và 63% HBeAg dương tính và HBeAg-âm tính những người nhận dùng adefovir. Không có đề kháng genotypic hoặc bùng phát virus liên quan đến đề kháng đã được nhìn thấy trong mỗi nhóm bệnh nhân nhận được tenofovir. Dữ liệu 72 tuần gần đây từ Hiệp hội châu Âu về gan năm 2008 chứng minh rằng HBV DNA không phát hiện được bởi phân tích hướng về điều trị là 79% bệnh nhân HBeAg dương tính và và 91% HBeAg âm tính trong trong nhánh dùng tenofovir đầu tiên, trong khi đó những bệnh nhân ban đầu được “chọn” dùng adefovir ở nhánh khác khi chuyển sang tenofovir từ tuần 48-72. Tỉ lệ HBV DNA không phát hiện được vẫn cao hơn trong phân tích những bệnh nhân thật sự điều trị. Những nghiên cứu kéo dài, đó là trong quá trình tiếp theo, cần cung cấp thông tin có giá trị về thông tin đề kháng của tenofovir theo thời gian. Tenofovir chưa được chấp thuận để điều trị viêm gan B tại Hoa Kỳ nhưng đã nhận được một ý kiến tích cực từ Ủy ban Thuốc dùng cho người của Cơ quan Thuốc châu Âu đối với sự chấp thuận để điều trị viêm gan B mãn tính ở người lớn.
C.Hướng dẫn cho việc lựa chọn đơn trị liệu ban đầu
Tại thời điểm hiện tại, các tiêu chuẩn để lựa chọn thuốc nào để sử dụng cho những bệnh nhân viêm gan B mãn tính nên tập trung vào việc đạt được sự ức chế virus nhanh chóng, mạnh mẽ với một nguy cơ đề kháng đi kèm tối thiểu. Với các tiêu chí được quan tâm này, cả hai hướng dẫn AASLD và bảng hướng dẫn chuyên sâu đã xuất bản một phác đồ đề nghị (đôi khi được gọi là “phác đồ Mỹ”) đồng ý rằng lamivudine đơn trị liệu nên tránh dùng như là một chế độ điều trị đầu tiên. Những trường hợp ngoại lệ có thể sử dụng lamivudine như là dự phòng chống lại sự tái hoạt động của virus ở những người HBsAg không hoạt động mà nhận hóa trị hoặc trong ba tháng cuối của thai kỳ- thời điểm mà ghi nhận theo dõi an toàn của nó được biện minh cho việc sử dụng này để ngăn ngừa lây truyền chu sinh. Tuy nhiên, trong thai kỳ nhà lâm sàng nên biết rằng cả telbivudine và tenofovir là thuốc nhóm B và, do đó khả năng chấp nhận là tương đương nhau mặc dù nhiều dữ liệu có sẵn hơn về việc sử dụng trong thai kỳ (có vài trăm trường hợp mang thai trong cơ sở dữ liệu tenofovir, được xuất phát từ việc sử dụng trong việc nhiễm HIV).
Hai thuốc uống được liệt kê trong các hướng dẫn AASLD như là nhữnng lựa chọn ưu tiên đầu tiên với việc bổ sung peginterferon alfa-2a- mà chính nó vẫn còn là một phương pháp tiếp cận đầu tiên cho cả các bệnh nhân HBeAg dương tính và HBeAg âm tính, là entecavir và adefovir. Tenofovir hiện nay chưa được phê duyệt để điều trị HBV, nhưng nó đem lại một tỉ lệ ức chế virus cao hơn nhiều so với adefovir trong những thử nghiệm 1 năm quan trọng, nên khi phê duyệt Tenofovir nên thay thế adefovir như là một chất nucleotide tương tự được ưu tiên sử dụng cho điều trị lần đầu.
Telbivudine không được khuyến cáo như là một loại thuốc đầu tay trong các hướng dẫn của AASLD gần đây nhất. Nó có hoạt tính chống virus tiềm năng với liều đã được phê duyệt là 600 mg / ngày và liều này thì cao cấp hơn so với lamivudine, và dữ liệu đề kháng của nó thì tốt nhất cho những bệnh nhân đạt được HBV DNA không thể phát hiện ở 24 tuần. Nếu telbivudine được chọn là liệu pháp ban đầu, thì mức HBV DNA nên được theo dõi cẩn thận, và nên có sự cân nhắc nhiều về việc thay đổi trong kế hoạc điều trị nếu có virus trong máu được phát hiện bất kỳ tại Tuần 24.
III. ĐƠN TRỊ LIỆU SO SÁNH VỚI PHỐI HỢP TRỊ LIỆU
Việc quan sát sự xuất hiện đề kháng đối với điều trị HBV, và kinh nghiệm tích lũy với điều trị HIV đã dẫn đến ý kiến cho rằng sự điều trị phối hợp đối với HBV nên là thường qui. Tuy nhiên, sự tiến triển chậm hơn rất nhiều của đề kháng HBV và các báo cáo gần đây về các tỉ lệ thấp đề kháng khi điều trị kéo dài của các thuốc mới hơn đã tạm dừng khái niệm điều trị phối hợp thường qui trong khi thiếu các dữ liệu hỗ trợ mạnh mẽ hơn cho thấy một lợi ích hơn của loại điều trị này ở hiệu quả hay đề kháng.
Trong việc ủng hộ quan niệm về điều trị kết hợp đối với HBV, có dữ liệu chứng minh khả năng làm giảm sự đề kháng của lamivudine khi nó được kết hợp với adefovir trong 2 năm so với lamivudine sử dụng một mình. Ngoài ra còn có dữ liệu chứng minh việc tăng cường khả năng ức chế virus khi nucleoside analogue emtricitabine được kết hợp với adefovir so với adefovir sử dụng đơn độc ; tuy nhiên, những phát hiện từ nghiên cứu này có thể chỉ đơn giản phản ánh hiệu quả của các thuốc mạnh hơn (như emtricitabine), những thuốc chưa được đánh giá như một đơn trị liệu trong nghiên cứu này. Ngược lại, thử nghiệm giai đoạn II của telbivudine với đặc điểm là 3 nhóm: lamivudine đơn trị, telbivudine đơn trị, và telbivudine kết hợp với lamivudine. Mức độ ức chế virus sau 1 năm không cao hơn với điều trị phối hợp so với telbivudine. Mặc dù các nhà điều tra đã không chắc chắn lý do tại sao trong trường hợp này, có vẻ như thận trọng để tránh sử dụng thuốc có đề kháng chéo, chẳng hạn như kết hợp lamivudine và telbivudine. Dùng với nhau, những dữ liệu còn hạn chế này không đủ để tạo ra một tiêu chuẩn mới cho việc sử dụng thường quy điều trị phối hợp ở thời điểm hiện nay.
Đối với những người thúc đẩy lý lẽ cho việc điều trị kết hợp thì cách lý tưởng để tổng hợp nó trong những hướng dẫn dựa trên bằng chứng đã được thực hiện trong một thử nghiệm ngẫu nhiên, dài hạn có kiểm chứng kiểm tra giả định rằng có thực sự là ít đề kháng với điều trị phối hợp hơn so với đơn điều trị. Đây là một bước ngoặc lớn với các đơn trị liệu hiện đang có sẵn vì nguy cơ cộng dồn rất nhỏ của đề kháng với một loại thuốc như entecavir cho dù lên đến 4 hoặc 5 năm. Vì vậy, có vẻ như nhiều khả năng rằng mục tiêu của cuộc thử nghiệm điều trị phối hợp hiện tại được bắt đầu hoặc dự tính sẽ thực hiện là cuộc trình diễn một số lợi ích khác mà có thể yêu cầu một khoảng thời gian ngắn hơn (ví dụ, tỷ lệ lớn hơn trong việc ức chế HBV DNA, chuyển đổi huyết thanh HBeAg, làm sạch HBsAg hoặc giảm nhanh chóng hơn nồng độ HBsAg, làm sạch nhanh chóng cccDNA, và có thể có khả năng ngừng điều trị mà không bị tái phát, đặc biệt ở bệnh nhân HBeAg-âm tính, vào những thời điểm xác định). Điều đó không có nghĩa là một điều chắc chắn rằng kết quả đó sẽ đạt được trong nay mai bởi vì cho đến nay chưa có bất kỳ một chứng minh nào của các điểm cuối với một chế độ kết hợp 2 loại thuốc mạnh hơn có sẵn.
Ngay cả khi không có những hướng dẫn dựa trên bằng chứng, một số bác sĩ vẫn thường xuyên chọn sử dụng liệu pháp kết hợp , trong trường hợp này có vẻ như việc kết hợp một nucleoside và nucleotide có thể là một kế hoạch hợp lý để tránh khả năng đề kháng chéo. Những trường hợp có lợi của ứng dụng này có thể được thực hiện mạnh nhất cho những bệnh nhân được phân loại sau đây, phân loại mà sự xuất hiện đề kháng đem đến nguy cơ lớn nhất.
1. Đề kháng được xác định đối với một thuốc. Những dữ liệu hiện tại với adefovir và lamivudine trong các thiết lập của đề kháng lamivudine cho thấy điều trị phối hợp phải luôn luôn được sử dụng trong hai thuốc này, bởi vì những thông tin đề kháng adefovir đã thất bại điều trị khi được dùng đơn trị liệu đã được ghi nhận ở đây. Bằng cách loại suy, cho dù không có dữ liệu được công bố, nhiều nguyên nhân của các chuyên gia cho rằng sự đề kháng đã được xác định đối với bất kỳ loại thuốc kháng HBV thì nên điều trị bằng liệu pháp kép.
2. Xơ gan. Đặc biệt là xơ gan tiến triển, nó rất quan trọng để tránh đề kháng do nguy cơ mất bù sau một viêm gan bùng phát.
3. Đồng nhiễm HIV / HBV. Những hướng dẫn gần đây cho thấy HBV ở những bệnh nhân này luôn luôn cần được điều trị trong tình trạng điều trị retrovirus hoạt tính cao, thường là với một chế độ điều trị có tenofovir, bất kể số lượng CD4. Entecavir đơn trị liệu gần đây đã cho thấy hoạt tính ức chế thích hợp chống lại HIV để được chọn cho những đột biến mà gây nên sự kháng lamivudine.
IV.KHI NÀO THAY ĐỔI ĐIỀU TRỊ?
Phương pháp truyền thống để điều trị sớm một bệnh nhân HBV trong thời đại của các thuốc uống là theo dõi từng thời điểm suốt quá trình điều trị mức HBV DNA, ALT, và tình trạng lâm sàng. Vào cuối những năm 1990, không lâu sau khi lamivudine ra đời, nhiều chú ý đã tập trung vào việc lamivudine nên tiếp tục hay không sau khi xuất hiện đề kháng. Có một quan điểm chung là lamivudine thực sự cần được tiếp tục trong khi đã có đề kháng thì dựa trên dữ liệu ban đầu cho thấy rằng làm như vậy đã đem lại việc giảm mức virus và ALT, khiến một số người kết luận sai lầm rằng bệnh nhân được tốt hơn hẳn với virus YMDD so với virus chủng hoang dại (wild-type virus). Khi được quan sát cho thấy rằng đột biến tiếp sau đó xuất hiện ở những vị trí gen khác trong DNA polymerase, lập lại tình trạng tái phát, nó trở nên rõ ràng rằng kết luận này không hợp lý. Sự phát triển tiếp theo của các thuốc với dữ liệu đề kháng tốt hơn đã đưa đến việc tranh luận khái niệm của việc đơn trị liệu tiếp tục chống lại những HBV đã phát triển đề kháng.
Những dữ liệu adefovir trước đây cho rằng một chuyển đổi sang thuốc này trong các trường hợp đã xác định đề kháng lamivudine được chỉ định, như khi hoạt động kháng virus của adefovir xuất hiện cũng tương tự đã được thấy chống lại HBV type hoang dại. Điều gì đã bị đánh giá thấp vào thời điểm đó, nhưng đã xuất hiện nhiều hơn gần đây, là thông điệp cân nhắc về hồ sơ đề kháng ở thời điểm từ 1 đến 2 năm của adefovir ở những bệnh nhân đề kháng lamivudine không giống như ở những người bị nhiễm típ hoang dại, lên đến 25% bệnh nhân kháng lamivudine phát triển đề kháng genotypic đối với adefovir trong vòng 2-3 năm. Các nghiên cứu của Lampertico và những người khác đã giới thiệu một cây dữ liệu chỉ ra rằng adefovir được thêm với lamivudine thay vì thay thế nó ở bệnh nhân đề kháng lamivudine thì hiếm xảy ra đề kháng adefovir xuất hiện trong vòng 3 năm đầu. Dữ liệu cũng cho thấy rằng adefovir có nhiều khả năng mang lại sự ức chế virus đến mức không thể phát hiện nếu nó được thêm vào khi mức HBV DNA ở bệnh nhân đề kháng lamivudine là thấp, đặc biệt là trước khi ALT bùng phát xảy ra.
1.Quản lý điều trị HBV hoạt động lại
Có một thay đổi theo hướng khác khiến tạo một cơ hội hoạt động lại trong điều trị khi ALT bùng phát xảy ra do sự xuất hiện của đề kháng hướng đến sự bùng phát virus như điểm đánh dấu sự hoạt động lại . Sau sự chuyển đổi này và trong tia sang của dữ liệu như những trích dẫn trên, các kết luận hợp lý là có thể tốt hơn để thay đổi điều trị khi đề kháng genotypic đầu tiên xảy ra và trước khi virus bùng phát. Điều này là do virus bùng phát có thể dự đoán trong hầu hết các tình huống mà đề kháng genotypic xảy ra, dẫn đến mức đề khántg virus cao hơn mà sau đó phải được ức chế.
Với những xét nghiệm tuần tự về gen có độ nhạy cao mà khả năng kinh tế sẵn có, và giả định rằng nhà lâm sàng có đủ kiến thức để giải thích kết quả, thì khôn ngoan là để kiểm tra đề kháng genotypic khi có virus còn tồn tại tại một số điểm thời gian phù hợp với một khả năng đề kháng có ý nghĩa thống kê có thể xảy ra. Ví dụ, nếu một bệnh nhân dùng lamivudine hoặc telbivudine có bất kỳ mức độ virus máu đước phát hiện tại 1 hoặc 2 năm, hoặc nếu một bệnh nhân dùng adefovir mà có virus máu phát hiện tại năm 2 hoặc 3, xét nghiệm đề kháng genotypic là thích hợp ngay cả nếu bệnh nhân không gặp những xác định cổ điển của việc bùng phát virus (tức là, gia tăng HBV DNA > 1 log10 với mức thấp nhất). Nếu đề kháng genotypic được phát hiện, điều trị với các thuốc ban đầu nên được tiếp tục và một loại thuốc không có đề kháng chéo nên được bổ sung, ví dụ, một nucleotide được thêm vào một nucleoside hoặc ngược lại. Phải được thừa nhận rằng đây là một ngoại suy cho tất cả các trường hợp đề kháng từ các tài liệu cụ thể liên quan đến kháng lamivudine, nhưng về mặt sinh học việc đối lập nhau thì thúc đẩy nhau.
2.Dự đoán đề kháng và chủ động giải quyết HBV trong quản lý điều trị
Gần đây, đã có một sự thay đổi sâu sắc trong suy nghĩ về cách tiếp cận tái phát kinh điển- một trong đó nhấn mạnh việc phát hiện sớm đề kháng genotypic –để tiếp cận giải quyết chủ động mà quy cho ưu tiên cao để tránh sự phát triển của đề kháng genotypic, bùng phát virus ít hơn nhiều vì đề kháng genotypic. Điều này đã được dựa trên dữ liệu với một số loại thuốc tương ứng mức virus HBV còn sót lại tại các thời điểm quan trọng được đo lường như việc ức chế hoàn toàn HBV DNA, chuyển đổi HBeAg huyết thanh, và xuất hiện đề kháng tại các điểm thời gian tiếp theo. Trong một nghiên cứu các bệnh nhân được điều trị lamivudine, Yuen và các đồng nghiệp đã chứng minh rằng nếu HBV DNA không bị phát hiện (< 103 bản sao / mL) ở 24 tuần thì 13% bệnh nhân có bùng phát virus do đề kháng ở trung bình tuần 120, so với 63% những người có mức HBV DNA ≥ 103 copies / mL tại Tuần 24 . Trong thử nghiệm quan trọng của adefovir, chỉ có 4% những người có HBV DNA không phát hiện được (<103 bản sao / mL) tại Tuần 48 đã đề kháng sau 4 năm so với hơn 40% những người có HBV DNA ≥ 103 copies/ mL tại Tuần 48. Giá trị tiên đoán của mức HBV DNA huyết thanh trong điều trị sớm như có thể là tuần 4 gần đây đã được đánh giá cho các bệnh nhân tiếp nhận điều trị lamivudine. Yuen và các đồng nghiệp xác định mức độ HBV DNA trong huyết thanh lúc ban đầu, lúc tuần thứ 2, 4, 8, 12, 16, 24, và 32, và hàng năm cho đến năm thứ 5 của 74 bệnh nhân viêm gan virus B mãn tính có HBeAg dương tính được điều trị bằng lamivudine. Vào năm 5, 17 bệnh nhân đã đạt được một "đáp ứng lý tưởng", được định nghĩa là mức độ HBV DNA < 400 IU / mL, chuyển đổi huyết thanh HBeAg, mức ALT bình thường, và không có đột biến YMDD. Phân tích các yếu tố tiên đoán của phản ứng cho thấy HBV DNA trong huyết thanh sớm như có thể là tuần 4 đã là một đáp ứng tiên đoán lý tưởng vào năm thứ 5. Mặc dù nghiên cứu này không gợi ý cho rằng nên phục hồi lại vai trò cho lamivudine như điều trị đầu tay, nhưng những kết quả nhấn mạnh một khái niệm quan trọng trong động học của virus HBV trong quá trình điều trị mà nên phục vụ như là một mô hình cho các nghiên cứu lâm sàng bổ sung thêm về các mô hình tiên đoán các đáp ứng rất sớm với các loại thuốc mới hơn.
Cơ sở dữ liệu lớn nhất đánh giá khái niệm này xuất phát từ thử nghiệm GLOBE, so sánh telbivudine và lamivudine ở những bệnh nhân HBeAg dương tính và HBeAg âm tính. Những bệnh nhân đã được phân tầng thành 4 nhóm khác nhau dựa trên mức độ HBV DNA ở tuần 24 của điều trị . Có một tỷ lệ cao đề kháng tại tuần 92 với lamivudine nhiều hơn telbivudine. Trong một phân tích một nhóm nhỏ của những bệnh nhân nhận được telbivudine, những bệnh nhân HBeAg-dương tính với HBV DNA < 109 copies / ml và ALT trên 2 lần giới hạn trên của bình thường cho thấy có một tỉ lệ đề kháng 2% tại tuần lễ 104 nếu HBV DNA đã không thể phát hiện tại Tuần lễ 24, trong khi bệnh nhân HBeAg-âm tính với HBV DNA ban đầu < 107 copies / mL có tỷ lệ đề kháng ở tuần 104 là 1,8% nếu HBV DNA âm tính ở tuần 24.
Từ những dữ liệu này xuất hiện khái niệm rằng nếu lamivudine hoặc telbivudine được chọn là liệu pháp ban đầu, trái với nguyên tắc đồng thuận hiện tại, chúng vẫn chấp nhận được như là lựa chọn điều trị chỉ khi HBV DNA là không thể phát hiện ở Tuần 24.Ngay cả virus máu còn ít tại Tuần 24 cũng liên quan với một tỷ lệ không thể chấp nhận đề kháng tiếp theo tại 1 và 2 năm (và, trong trường hợp dùng lamivudine, một luận cứ mạnh mẽ có thể được thực hiện là tỷ lệ đề kháng tiếp theo là không thể chấp nhận ngay cả khi HBV DNA là không thể phát hiện tại 24 tuần, nhấn mạnh điều không phù hợp của nó như là một loại thuốc đầu tay). Hơn nữa, dữ liệu từ thử nghiệm GLOBE đã chứng minh rằng các đặc điểm ban đầu như mức HBV DNA thấp và mức độ ALT cao có thể giúp dự đoán khả năng đề kháng telbivudine tối thiểu khi kết hợp quan sát về các mô hình đáp ứng điều trị một lần đã bắt đầu.
Với các loại thuốc có rào cản di truyền cao hơn đối với đề kháng (như entecavir và tenofovir), có ít dữ liệu liên kết giá trị tiên đoán của mức HBV DNA đến hiệu quả lâu dài ở bệnh nhân tình nguyện điều trị vì tỷ lệ đề kháng rất thấp được báo cáo đến nay đối với các thuốc này. Entecavir đặc biệt gần đây đã báo cáo có tỷ lệ đề kháng genotypic lâu dài là 1,2% sau 5 năm ở bệnh nhân tình nguyện điều trị, mặc dù những người này vẫn có một số đặc điểm của thiết kế chương trình (với không phải tất cả bệnh nhân được theo dõi điều trị đủ thời gian và với những bệnh nhân được chuyển sang một liều 1,0 mg từ 0,5 mg), cho thấy rõ ràng một hồ sơ kháng mạnh mẽ, Những dữ liệu đề kháng chiến lâu dài trên tenofovir là cần thiết, nhưng sự vắng mặt của bất kỳ kháng genotypic trong cuộc thử nghiệm quan trọng tại 1 năm là hứa hẹn.
3.Các bước tiếp cận trong điều trị
Với những nhận xét này, một ban chuyên gia đã xuất bản cái nó được gọi là một “lộ trình” tiếp cận trong năm 2007, đề xuất rằng thời điểm quan trọng đầu tiên để đánh giá ở một bệnh nhân bắt đầu điều trị kháng virus là 12 tuần , tại thời điểm này đáp ứng < 1 log10 ở bệnh nhân phù hợp cũng phải được xem như là một ”người không đáp ứng nguyên phát” mà phải đưa đến một thay đổi trong điều trị.
Thời điểm quan trọng kế tiếp trong lộ trình tiếp cận là 24 tuần điều trị, khi mà việc đạt được một đáp ứng “hoàn thành” (được định nghĩa là không thể phát hiện HBV DNA bằng PCR) quyết định cho việc tiếp tục điều trị với các thuốc hiện tại . Đối với những bệnh nhân đạt được một đáp ứng virus hoàn tất vào thời điểm này, bảng điều khiển đề nghị nên theo dõi với những khoảng 6 tháng.
Quản lý tiếp theo đáp ứng virus tuần 24
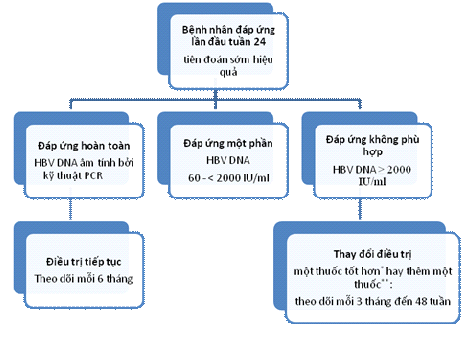
* Nếu có khả năng
**Theo dõi định kỳ có thể kéo dài 6 tháng đến 48 tuần dựa vào việc đạt được HBV DNA không phát hiện được theo chỉ định của bác sĩ. Những bệnh nhân có bệnh phối hợp nên được theo dõi mỗi 3 tháng phụ thuộc vào đáp ứng virus.
Ở điểm cuối khác của sự phân bố những đáp ứng có thể tại Tuần 24 là bệnh nhân có một đáp ứng “không đầy đủ” (định nghĩa là mức độ HBV DNA> 2.000 IU / mL). Bảng điều khiển cảm thấy rằng bệnh nhân trong nhóm này được đảm bảo một sự thay đổi trong điều trị: hoặc chuyển sang một loại thuốc mạnh hơn, nếu như một loại thuốc đã có sẵn, hoặc thêm một thuốc thứ hai, tốt hơn một mà không có đề kháng chéo với thuốc ban đầu đang được sử dụng tiếp tục. Ở những bệnh nhân này, bảng điều khiển đề nghị theo dõi mỗi 3 tháng cho đến 48 tuần, có thể được kéo dài đến 6 tháng khi vượt quá 48 tuần dựa trên việc đạt được không thể phát hiện HBV DNA. Tuy nhiên, những bệnh nhân bị bệnh đã tiến triển nên được theo dõi khoảng cách mỗi 3 tháng không phụ thuộc vào đáp ứng virus.
Ở những bệnh nhân HBV DNA trong khoảng trung bình 60- 2000 IU / mL tại Tuần 24 (còn gọi là đáp ứng "một phần"), "rào cản di truyền" đối với đề kháng (khó khăn hay dễ dàng như thế nào đối với HBV để trở nên đề kháng với một loại thuốc nhất định) xác định tiến trình hành động trong các bước tiếp cận . Với một loại thuốc được xem xét bởi bảng điều khiển mà có một rào cản di truyền thấp (chẳng hạn như lamivudine hoặc telbivudine), bảng điều ủng hộ phối hợp thêm một loại thuốc không có đề kháng chéo để ngăn chặn sự xuất hiện của đề kháng và bùng phát virus. Với một loại thuốc được coi là có một hàng rào di truyền cao đề kháng như adefovir hoặc entecavir, bảng điều khiển đề nghị tiếp tục điều trị với các thuốc hiện tại với giám sát bổ sung định lượng HBV DNA mỗi 3 tháng cho đến 48 tuần. Với adefovir, nếu đáp ứng vẫn là một phần hay trở thành không đầy đủ thì một thay đổi trong điều trị phải được thực hiện (hoặc thêm vào hoặc chuyển sang một thuốc mạnh hơn). Với entecavir hoặc tenofovir, chúng ta thiếu dữ liệu đầy đủ để thực hiện các khuyến cáo dứt khoát về sự cần thiết phải thay đổi chế độ điều trị nếu vẫn còn virus trong máu tại Tuần 48. Trong trường hợp của entecavir, hồ sơ đề kháng 5 năm là tốt, và các hồ sơ đề kháng lâu dài của tenofovir vẫn chưa được xác định. Nếu không phát hiện HBV DNA được thực hiện tại Tuần lễ 48, với một loại thuốc hàng rào di truyền cao, đơn trị liệu có thể được tiếp tục.
Xử trí Tuần 24 đối với đáp ứng một phần.
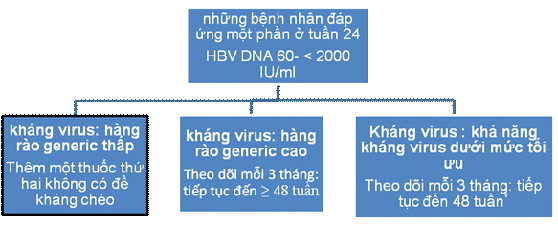
*Nếu đáp ứng không hoàn toàn ở tuần 48, thay đổi điều trị hay thêm một thuốc kháng virus nữa không có đề kháng chéo
4.Quản lý trong Điều trị: Chuyển đổi thuốc hay với Bổ sung thuốc?
Cách tiếp cận này không nên được coi như một đồ án cứng nhắc và trong một số trường hợp sử dụng thuật ngữ khái quát như "điều trị nên được thay đổi" mà không ghi rõ chi tiết như liệu nên thêm hoặc chuyển đổi. Nó có thể là trường hợp đối với những bệnh nhân nhất định, bổ sung vào điều trị khi không có đề kháng genotypic có thể không cần thiết và một chuyển đổi thuốc có thể là thích hợp. Ví dụ: nếu một bệnh nhân dùng adefovir có HBV DNA ở giới hạn trên của đáp ứng một phần (60- 2000 IU / mL), một cách hợp lý có thể chuyển sang một loại thuốc mạnh hơn tại điểm đó. Cách tiếp cận này được hỗ trợ bởi các kết quả xuất sắc được báo cáo trong những trường hợp của những bệnh nhân đáp ứng dưới tối ưu đối với adefovir , là những người chuyển sang tenofovir cũng như 2 báo cáo nghiên cứu gần đây, những báo cáo mà bệnh nhân chuyển từ adefovir sang tenofovir tại Tuần 48 nhanh chóng đạt được đáp ứng virus mạnh. Lợi ích của việc chuyển là những bệnh nhân có đáp ứng dưới mức tối ưu hoặc kháng adefovir đến cả entecavir cũng đã được mô tả trong những nghiên cứu nhỏ với entecavir 1 mg / ngày.
Các dữ liệu lớn nhất được thiếp lập để đánh giá vấn đề này xuất phát từ việc nghiên cứu ngẫu nhiên giai đoạn IIIb của những bệnh nhân HBeAg dương tính tình nguyện dùng nucleoside trong đó một nhóm bệnh nhân đã được dùng ban đầu với adefovir 24 tuần tiếp theo là chuyển đổi thành telbivudine 28 tuần bất kể đáp ứng (n = 46), trong khi những bệnh nhân ở một nhóm khác đã nhận được adefovir cho 52 tuần. HBV DNA trung bình đã giảm khoảng 1,4 log10 copies/ mL giữa tuần 28 và 52 trong nhóm chuyển sang telbivudine, kết quả HBV DNA trung bình tại Tuần lễ 52 thấp hơn có ý nghĩa đáng kể so với ở những bệnh nhân vẫn còn dùng adefovir (3,01 so với 4,00 log10 copies / mL, P = 0,004). Mặc dù đã có nhiều bệnh nhân không thể phát hiện HBV DNA trong nhóm chuyển đổi hơn trong nhóm adefovir 52 tuần, sự khác biệt này đã không đạt được ý nghĩa thống kê (54% so với 40%, P = 0,20). Tỷ lệ thất bại điều trị ban đầu (được xác định bởi protocol nghiên cứu khi mức HBV DNA còn lại > 5 log10 copies / mL cho đến tuần 52) là cao hơn đáng kể trong nhóm adefovir 52 tuần so với nhóm chuyển đổi (29% vs 11%, tỷ lệ odds: 0,30 [khoảng tin cậy 95%: 0,10-0,96; P = 0,042]). Một trong những liên quan đặc biệt, 78% người nhận adefovir đã có một đáp ứng dưới mức tối ưu tại Tuần 24 (mức HBV DNA ≥ 3 log10 bản sao / mL) ở cả 2 nhóm. Những người đáp ứng dưới mức tối ưu trong nhóm chuyển đổi cho thấy một giảm trung bình HBV DNA thêm vào là -2,1 log10 bản sao / mL giữa tuần 24 và 52, so với 0,8 log10 bản sao / mL cho những bệnh nhân vẫn còn dùng adefovir.
Nhìn chung, có một xu hướng giữa các chuyên gia thiên hướng tới việc sử dụng liệu pháp kết hợp ở những bệnh nhân đáp ứng chưa đầy đủ đối với một đơn trị liệu thay vì chuyển đổi không phải vì điều này đã chứng minh việc ức chế virus được hỗ trợ mà giảm thiểu khả năng của nguy cơ lâu dài đối với đề kháng dựa trên những nguyên lý virus đã được kiểm chứng trong những thiết kế điều trị khác nhau cũng như HIV.
Đến bây giờ, khái niệm tiếp cận cũng phải được xem xét động mà nó sẽ tiến triển theo thời gian để có liên quan hợp lý đến thời điểm sớm hơn và đòi hỏi sự linh hoạt đáng kể dựa vào các đặc tính cá nhân của bệnh nhân và sự lựa chọn điều trị để được thực hiện. Đồng thời, nó cung cấp một khuôn khổ cho một cách tiếp cận chủ động để điều trị mà tối ưu hóa các đáp ứng và giảm thiểu sự đề kháng lâu dài ở ưu thế trội ở các bệnh nhân của chúng tôi, ngay cả khi sự phân bố bệnh nhân được dự đoán để thành ứng cử viện được điều trị đang mở rộng một cách đều đặn.
V.KHI NÀO THÌ DỪNG
Câu hỏi là khi nào ngừng điều trị chống viêm gan virus B bằng một nucleos (t) ide là một vấn đề mà phải phân biệt chính xác nhất các mục tiêu điều trị ở những bệnh nhân HBeAg dương tính và HBeAg âm tính. Mục tiêu thông thường ở cả hai nhóm bệnh nhân là ức chế virus mạnh và lâu dài. Theo định nghĩa, chuyển đổi huyết thanh HBeAg là duy nhất đối với những bệnh nhân HBeAg dương tính và là một điều kiện tiên quyết cho thấy sự ức chế virus đã thành công. Ngược lại, sự ức chế virus không đảm bảo rằng việc chuyển đổi huyết thanh HBeAg sẽ xảy ra. Khi nó xảy ra, nó đại diện cho một cơ hội ức chế virus lâu bền sau điều trị sau khi một thời gian điều trị có giới hạn mà điều đó không đúng trong trường hợp HBeAg-âm tính.
1.Bệnh nhân HBeAg- dương tính
Chuyển đổi huyết thanh xảy ra ở khoảng 10% đến 25% bệnh nhân trong vòng 3 năm mà không cần điều trị nucleos (t) ide. Một số yếu tố đã được tìm thấy liên quan với tỷ lệ cao hơn cho chuyển đổi huyết thanh bao gồm thời gian điều trị ngắn hơn (được định nghĩa là thời gian điều trị cho đến sau khi chuyển đổi huyết thanh HBeAg), tuổi lớn hơn, mức HBV DNA cao hơn ở thời điểm điều trị đã ngừng lại, và việc nhiễm HBV kiểu gen C thì cao hơn so với B. Tuy nhiên , đối với hầu hết bệnh nhân viêm gan B mãn tính, khả năng đảo ngược lại huyết thanh là thấp để đảm bảo ít nhất 1 cố gắng để không tiếp tục điều trị. Virus tái phát và đợt kịch phát của viêm gan có thể xảy ra sau khi ngưng điều trị và có thể biểu hiện trễ lên đến 1 năm sau khi ngưng điều trị. Kết luận là, ngoại trừ ngừng điều trị sau khi chuyển đổi huyết thanh HBeAg có thể ở bệnh nhân xơ gan, ở những người mà việc đảo ngược lần nữa huyết thanh và tái phát với mức độ virus cao có thể thúc đẩy xơ gan mất bù.[72] Vì nguyên nhân này, đã có đề xuất trong một số hướng dẫn là những bệnh nhân xơ gan nên tiếp tục điều trị vô hạn định cho đến khi họ đạt được sạch HBsAg.
Các bác sĩ lâm sàng điều trị cho bệnh nhân không xơ gan, những người đạt được chuyển đổi huyết thanh HBeAg lại phải đối mặt với những câu hỏi việc điều trị củng cố kéo dài trong bao lâu. Thêm sáu tháng đã trở thành một thời gian được chấp nhận rộng rãi sau khi điều trị chuyển đổi huyết thanh HBeAg đạt được, nhưng trong những trường hợp không gây hại do điều trị, nhiều bác sĩ lâm sàng thích điều trị ít nhất là 12 tháng nữa. Một số miễn cưỡng không tiếp tục điều trị, ngay cả sau 12 tháng điều trị bổ sung sau khi đã chuyển đổi huyết thanh nếu HBV DNA còn được phát hiện trong khoảng 102-103 IU /mL.
Các hướng dẫn AASLD khuyên nên theo dõi chặt chẽ những bệnh nhân được điều trị nucleos(t)ide và ngưng (mỗi 1-3 tháng trong 6 tháng đầu, và mỗi 3-6 tháng sau đó) và lưu ý rằng việc bắt đầu lại điều trị thường có hiệu quả trong việc kiểm soát bệnh gan tiến triển ở những bệnh nhân đã không xuất hiện đề kháng.
2.Bệnh nhân HBeAg-âm tính
Đối với bệnh nhân HBeAg-âm tính, có một nghịch lý quan trọng. Đó là dễ dàng hơn để đạt được HBV DNA không bị phát hiện so với ở những bệnh nhân HBeAg dương tính vì việc bắt đầu điều trị sớm với mức HBV DNA lúc ban đầu thấp hơn. Tuy nhiên, đa số bệnh nhân HBeAg-âm tính (> 95%) tái phát nếu điều trị không tiếp tục sau 1 năm, đưa đến việc tranh luận còn nhiều bàn cãi như là tranh luận ngưng tại thời điểm đó có nên không. Nhiều dữ liệu khuyến khích đến từ một báo cáo gần đây của Fung và các đồng nghiệp thực hiện trên 45 bệnh nhân HBeAg-âm tính đã ngưng lamivudine sau 2 năm điều trị trong thời gian đó họ được kiểm tra HBV DNA nhiều lần đều âm tính bởi kỹ thuật PCR. Tỷ lệ tái phát virus tại 24, 36, và 48 tháng sau khi ngừng điều trị là 50%, 62%, và 74%, tương ứng với từng thời gian. Vì vậy, từ một điểm sinh học làm xuất hiện các vấn đề quan trọng xảy ra ở một số bệnh nhân đã được điều trị kéo dài (ví dụ, cccDNA giảm hoặc một đáp ứng miễn dịch gia tăng) nhằm nâng cao tỷ lệ đáp ứng lâu bền.
Mặt khác, Hadziyannis và các cộng sự đã trình bày các kết quả của một nghiên cứu quan sát, trong đó họ theo dõi một cohort với 33 bệnh nhân HBeAg-âm tính từ một thử nghiệm quan trọng của adefovir, những người đã nghỉ điều trị sau 5 năm điều trị sau khi đã đạt HBV DNA âm tính. Tất cả nhóm người này đã tái phát (có virus lại trong máu). 11 trong số 33 trường hợp đã tăng ALT và được quay trở lại điều trị. Những người còn lại, virus trong máu sạch ở một phần ba trường hợp trong vòng 18 tháng, với virus trong máu thấp bị phát hiện trong hai phần ba khác. Ở đây, rõ ràng là điều trị dài hạn đem lại những lợi ích và cơ hội cho sự chấm dứt điều trị là không phát sinh với 1 năm điều trị. Tuy nhiên, đối với nhiều bác sĩ lâm sàng (bao gồm cả tác giả), tỉ lệ thấp của ức chế virus lâu bền và tình trạng gia tăng tái phát theo thời gian hiện cung cấp không đủ các căn cứ để biện minh cho ngừng thường quy đối với bất kỳ nucleos(t)ide analog có sẵn ở những bệnh nhân HBeAg-âm tính ngay cả sau 5 năm điều trị.
Tóm tắt: Ý nghĩa đối với thực hành lâm sàng:
• Hiệu quả điều trị HBV yêu cầu cả ức chế virus lâu dài và tránh các đề kháng xuất hiện.
• Vấn đề đầu tiên phải đối mặt trong việc quản lý các nhiễm viêm gan B mãn tính là loại thuốc nào được chọn như điều trị ban đầu: điều trị bằng interferon hoặc điều trị thuốc uống.
• Những thuận lợi của liệu pháp interferon bao gồm một khóa điều trị có giới hạn (tức là chỉ 1 năm điều trị), một tỷ lệ cao chuyển đổi HBeAg huyết thanh (ở bệnh nhân HBeAg dương tính), khả năng mất hoặc chuyển đổi huyết thanh đối với HBsAg, một tỷ lệ đáng kể đối với ức chế virus bền lâu, và ít phát triển đề kháng. Nhược điểm bao gồm một tỷ lệ cao những tác dụng bất lợi liên quan đến điều trị.
• Những thuận lợi của điều trị thuốc uống bao gồm tỉ lệ cao chuyển đổi HBeAg huyết thanh với điều trị kéo dài, khả năng mất hoặc chuyển đổi huyết thanh đối với HBsAg với việc sử dụng các thuốc mới có khả năng mạnh, và khả năng dung nạp rất tốt. Bất lợi bao gồm sự cần thiết phải tiếp tục điều trị không xác định thời hạn và tiềm năng xuất hiện đề kháng.
• Entecavir và tenofovir có dữ liệu đề kháng rất tốt ở những bệnh nhân tự nguyện điều trị. Dữ liệu đề kháng của Telbivudine là xuất sắc trong các nhóm nhỏ những bệnh nhân như là những người với HBV DNA không thể phát hiện ở tuần 24 và một số thông số xác định với ALT (cao) và HBV DNA (thấp) lúc ban đầu.
• Các thuốc hiện đang khuyến cáo như là sự lựa chọn đầu tiên trong các hướng dẫn AASLD cho bệnh viêm gan B bao gồm peginterferon alfa-2a, entecavir, và adefovir. Lamivudine không nên được sử dụng như một loại thuốc hàng đầu vì dữ liệu đề kháng kém của nó. Tenofovir có khả năng sẽ thay thế adefovir .
• Có những dữ liệu chưa đầy đủ khuyên bạn nên kết hợp một chế độ điều trị chuẩn cho các bệnh nhân tự nguyện điều trị hoặc những bệnh nhân cần điều trị tại thời điểm hiện nay. Nếu quyết định được thực hiện là điều trị kết hợp ngay từ đầu, một nucleoside và một nucleotide nên được sử dụng với nhau để tránh khả năng đề kháng chéo.
• Điều trị phối hợp có thể được tốt cho các bệnh nhân với đề kháng đã được xác định đối với 1 thuốc, xơ gan, đồng nhiễm HIV / HBV, và / hoặc phản ứng yếu đối với một loại thuốc HBV ban đầu.
• Thận trọng theo dõi định kỳ đối với vấn đề đề kháng genotypic ở bệnh nhân khi phát hiện còn virus trong máu trong quá trình điều trị. Nếu đề kháng được phát hiện, thêm một thuốc kháng virus khác hiện nay để tránh sự bùng phát virus có thể xảy sau nhanh chóng sau sự phát triển của đề kháng.
• Gần đây đã có một sự thay đổi sâu sắc trong suy nghĩ từ cách tiếp cận truyền thống đến việc tiếp cận chủ động mà hướng đến việc ưu tiên cao để tránh sự phát triển của kháng genotypic.
• Có thể dự đoán khả năng đề kháng phát triển của một số loại thuốc HBV theo thời dian dài dựa trên mức HBV DNA tại những thời điểm nhất định bao gồm 4, 12, 24 và 48 tuần.
• Phác đồ từng bước năm 2007 có thể được sử dụng như một tài liệu hướng dẫn điều trị cho việc quyết định những quản lý phù hợp của một bệnh nhân dựa trên những đáp ứng virus của họ tại tuần 12 và 24 và các rào cản đề kháng genotypic liên quan với các loại thuốc mà họ đang được điều trị.
• Đối với hầu hết bệnh nhân HBeAg dương tính đạt được chuyển đổi HBeAg huyết thanh, cơ hội đảo ngược lại là thấp (10% đến 20%) để đảm bảo một cố gắng không tiếp tục điều trị, cho dù điều trị nên được tiếp tục trong 6-12 tháng sau chuyển đổi huyết thanh để giảm nguy cơ của đảo ngược huyết thanh lại.
• Mặc dù tỷ lệ ức chế virus ở cá nhân HBeAg-âm tính điều trị thuốc uống cao với điều trị liên tục, nguy cơ cao tái phát khi ngừng điều trị thì đủ để biện minh cho việc không ngừng điều trị thường quy đối với các nucleos(t)ides có khả năng.